
【題目】現有失去標簽的4種固體物質,分別是BaCl2、BaCO3、Na2CO3和NaHSO4。
(1)在僅提供蒸餾水和所需儀器的條件下,鑒別出上述4種固體物質。
①最先鑒別出來的固體物質是_____。
②利用①中鑒別出來的物質又可直接鑒別出的固體物質是_____,依據的實驗現象是_____。
③利用②中鑒別出來的物質即可鑒別出其它物質。
(2)用鑒別出來的物質進行實驗:向Na2CO3溶液中滴入BaCl2溶液至恰好完全反應。
①觀察到的實驗現象是_____。
②下圖表示該反應前后溶液中存在的主要離子,寫出以下圖形代表的離子(填離子符號):
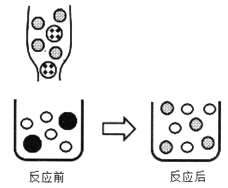
![]() _____
_____![]() _____
_____![]() _____
_____
【答案】BaCO3 NaHSO4 有氣泡產生 產生白色沉淀 Cl- Na+ CO32-
【解析】
(1)①NaHSO4、Na2CO3、BaCl2、BaCO3固體四種物質中只有碳酸鋇不溶于水,將四種物質分別加入水,不能形成溶液的是碳酸鋇,所以最先檢驗出來的固體物質是碳酸鋇;
②由于NaHSO4在水中會解離出Na+、H+、SO42-其中能組合成硫酸,硫酸能與碳酸鋇反應生成硫酸鋇沉淀、水和二氧化碳,所以有氣體放出的是硫酸氫鈉, 所以利用它又可直接檢驗出的固體物質是硫酸氫鈉;
(2)①向Na2CO3溶液中滴入BaCl2溶液至恰好完全反應生成碳酸鋇沉淀和氯化鈉,觀察到的實驗現象是產生白色沉淀;
②向Na2CO3溶液中滴入BaCl2溶液至恰好完全反應生成碳酸鋇沉淀和氯化鈉,反應的實質是碳酸根離子與鋇離子產生碳酸鋇沉淀,氯離子與鈉離子在反應過程中不變。![]() 表示氯化鋇溶液中反應后溶液中存在的氯離子,離子符號為:Cl-;
表示氯化鋇溶液中反應后溶液中存在的氯離子,離子符號為:Cl-;![]() 表示碳酸鈉溶液中反應后溶液中存在的鈉離子,離子符號為Na+:Na+;
表示碳酸鈉溶液中反應后溶液中存在的鈉離子,離子符號為Na+:Na+;![]() 碳酸鈉溶液中的碳酸根離子,離子符號為:CO32-。
碳酸鈉溶液中的碳酸根離子,離子符號為:CO32-。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
【題目】下圖為元素周期表的一部分。下列說法錯誤的是( )
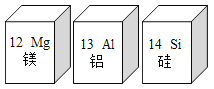
A. 一個鎂原子失去兩個電子變成Mg2+ B. 鋁原子核外有13個電子
C. 三種元素都是金屬元素 D. 鎂、鋁、硅的原子序數依次增加
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖是鈉元素和氯元素在元素周期表中信息和有關的4種粒子結構示意圖,下列說法正確的是( )
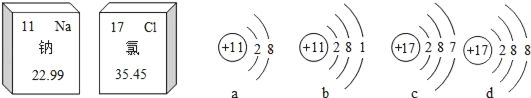
A. 鈉、氯都屬于金屬元素
B. 氯的相對原子質量是35.45g
C. 氯化鈉是由a、d兩種粒子構成的
D. c表示的是一種陰離子
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在H、C、O、Cl、Ca、Fe六種元素中,根據要求完成填空。
(1)選擇適當的元素,組成符合下列要求的物質,將其化學式填入空格中:
①可以用作燃料的氧化物是_____,②胃液中含有的酸____,
③可以改良酸性土壤的堿______
(2)用上述六種元素組成適當的物質,寫出符合下列要求的化學方程式:
①電解水的反應______
②天然氣燃燒的反應_______
③中和反應______
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列反應中屬于復分解反應的是
A. 3Fe + 2O2![]() Fe3O4B. 2KOH+H2SO4=K2SO4+2H2O
Fe3O4B. 2KOH+H2SO4=K2SO4+2H2O
C. H2 + CuO![]() Cu + H2OD. Fe2O3 + 3CO
Cu + H2OD. Fe2O3 + 3CO![]() 2Fe+3CO2
2Fe+3CO2
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某實驗小組利用石灰石殘渣(雜質不溶于水也不溶于酸)制備輕質CaCO3,同時得到K2SO4,其工藝流程簡要如下:
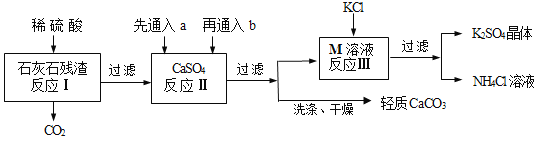
已知:CaCO3 + H2O + CO2 = Ca(HCO3)2
(1)為了提高反應Ⅰ的速率,下列措施中可行的是____(填序號);
①攪拌 ②將殘渣粉碎成細小顆粒 ③適當增大硫酸的濃度
(2)反應Ⅱ中a和b分別是____(填序號);
①足量CO2、適量NH3 ②足量NH3、適量CO2
③適量CO2、足量NH3 ④適量NH3、足量CO2
(3)反應Ⅲ中相關物質的溶解度如下表,該表中M物質的化學式為____,反應Ⅲ在常溫下能實現的原因是____,生成的NH4Cl溶液在農業上可用作____;
物 質 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)將得到的輕質CaCO3進行洗滌,判斷CaCO3固體已洗滌干凈的方法:取最后一次洗滌液,____(填序號),若無明顯的現象,則已洗凈;
①滴加稀鹽酸
②滴加Na2SO4 溶液
③滴加BaCl2溶液
(5)過濾器中的濾紙折疊方法如圖所示,正確的順序是____(填序號);
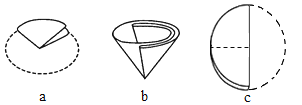
(6)該工藝流程中可循環利用的物質除H2O外,還有____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】回答下列與金屬有關的問題。
(1)黃銅片與銅片互相刻劃目的是_____;
(2)鋁比鐵活潑,但抗腐蝕性能卻更強,用化學方程式解釋其原因_____;
(3)工業上,把赤鐵礦冶煉成鐵的主要反應原理是3CO+Fe2O3![]() 2Fe+3CO2,其中_____發生了氧化反應。
2Fe+3CO2,其中_____發生了氧化反應。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據實驗裝置圖,回答下列問題:

(1)用過氧化氫溶液和二氧化錳混合制取氧氣應選用的發生裝置是___;反應方程式為____
(2)實驗室制取CO2和收集二氧化碳氣體應選擇的裝置是___;
(3)如裝置F所示,點燃兩支短蠟燭,然后沿燒杯內壁傾倒二氧化碳時,看到F中的實驗現象是__________;
(4)某同學選用G裝置進行實驗,看到與上一步實驗F的實驗現象___(填“相同”或“不同”);
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com