
【題目】金屬材料廣泛應用于生產生活中。
(1)鋁在空氣中與氧氣反應,其表面生成一層致密的氧化物薄膜,從而阻止鋁進一步氧化。這種氧化物的化學式為_____________。
(2)向含有氯化銅、氯化鋅、稀鹽酸的混合溶液中加入過量鐵粉,充分反應后過濾,濾液中含有的溶質是_____________(寫化學式)。
(3)鐵礦石有多種,如赤鐵礦(主要成分 Fe2O3)和磁鐵礦(主要成分 Fe3O4)等。寫出磁鐵礦石中的主要成分與一氧化碳反應的化學方程式_____________。
(4)含有鋅粉 6.5g、鐵粉 5.6g、銅粉 3.2g、鋁粉 l.8g 的混合物與一定質量的稀硫酸充分反應,反應停止后,有 6g 固體剩余。則生成氫氣的質量為____________g。
【答案】Al2O3 FeCl2、ZnCl2  0.5g
0.5g
【解析】
(1)鋁在空氣中與氧氣反應,鋁與氧氣反應生成氧化鋁,氧化鋁是一層致密的氧化鋁薄膜,可以阻止鋁進一步氧化。氧化鋁的化學式為Al2O3。故答案為:Al2O3;
(2)由金屬活動性順序表可知,鋅>鐵>氫>銅。在氯化鋅、氯化銅、鹽酸的混合溶液中加入過量的鐵粉。鐵與稀鹽酸反應生成氯化亞鐵和氫氣,鐵能將氯化銅全部反應生成氯化亞鐵和銅,不能與于氯化鋅反應。充分反應后過濾,濾液中不含氯化銅,生成氯化亞鐵。且溶液中還有未被反應的氯化鋅。故答案為:FeCl2、ZnCl2;
(3)磁鐵礦的主要成分是四氧化三鐵,一氧化碳和四氧化三鐵在高溫下反應,生成鐵和二氧化碳。故答案為: ;
;
(4)因為Cu不能與稀硫酸發生置換反應,所以剩余的6g固體中一定含有3.2g的銅粉。因為鐵、鋅、鋁的活動性順序為:鋁>鋅>鐵>氫,所以鋁、鋅優先反應,鐵再發生反應。所以除了銅外,剩余固體為6g-3.2g=2.8g的鐵粉。則1.8g的鋁、6.5g的鋅、5.6g-2.8g=2.8g的鐵和硫酸反應了。
設鋅與硫酸反應生成氫氣的質量為x,鐵與硫酸反應生成氫氣的質量為y,鋁與硫酸反應生成氫氣的質量為z。

解得x=0.2g

解得y=0.1g
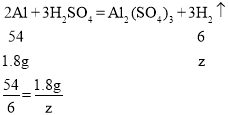
解得z=0.2g
則可得氫氣的質量為:0.2g+0.1g+0.2g=0.5g。
故答案為:0.5g。


科目:初中化學 來源: 題型:
【題目】如圖是甲、乙兩種物質的溶解度曲線。在t2℃時往盛有100g水的燒杯中先后加入20g甲和20g乙(兩種物質溶解時互不影響,且溶質仍是甲、乙),充分攪拌。將混合物的溫度降低到t1℃。下列說法正確的是
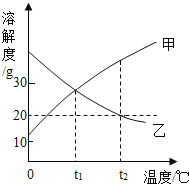
A.甲物質的溶解度受溫度變化的影響較大,乙物質的溶解度受溫度變化的影響較小
B.要使乙從其濃溶液中析出,可采用冷卻熱飽和溶液法
C.溫度降低到t1℃時,甲、乙的溶質質量分數相等
D.t2℃時,甲物質的溶液為飽和溶液,乙物質的溶液為不飽和溶液
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】2020年2月8日,武漢市為抗擊新冠肺炎疫情,緊急搭建的第二所醫院雷神山醫院交付使用,雷神山醫院在建造過程中使用了大量的活動板房,活動板房是以彩鋼為骨架,以夾芯板為圍護材料,全新概念的環保經濟型房屋,請回答:

(1)作為活動板房骨架的彩鋼屬于_____(填字母)。
A 金屬材料
B 無機非金屬材料
C 復合材料
施工過程中使用的挖掘機的鏟斗可以選用的材料是_____(填字母)。
A 韌性好、硬度大的錳鋼
B 抗腐蝕性好、密度小的純鋁
C 可塑性好、機械性能好的鈦合金
(2)挖掘機的能量來源是柴油,在其工作過程中的能量轉化_____。
(3)建造過程要用到玻璃,工業上制造玻璃的一個反應原理可以表示為:純堿和二氧化硅在高溫條件下反應,生成硅酸鈉和一種用于滅火的氣體,反應中不存在元素化合價的變化且硅酸根為-2價,則該反應的化學方程式為_____。
(4)在修建的工地上,由于大量土方的使用,空氣中_____(填一種空氣污染物)的含量會明顯增加,為了減小對身體健康的影響,建筑工人們一般施工時都戴有口罩。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據初中化學知識素養。請回答下列問題。
(1)下列各組微粒中:
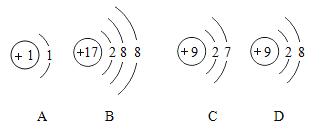
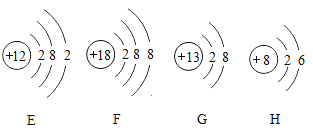
①上述微粒結構示意圖表示陰離子的是____________(填序號)
②上述結構示意圖,達到穩定結構的原子是____________(填序號)
③C和E兩種元素形成化合物的化學式為____________.
(2)A、B、C 三種固體物質在水中的溶解度曲線如圖所示,請回答:
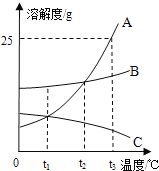
①在t1℃時,A、B兩種物質達到飽和狀態時溶解的質量______(填 “一定相等”、“一定不相等”或“可能相等”);
②若B中混有少量的A,最好采用_________的方法提純B;
③現有接近飽和的C物質溶液,使其變成飽和溶液的方法有:加入C物質;恒溫蒸發溶劑;________________;
④t3℃時將20g A物質放入50g水中,充分攪拌,所得溶液中溶質的質量分數是_____;
⑤將 t3℃時等質量的 A、B、C 三種物質的飽和溶液降溫至 t1℃時,所得溶液的溶質質量分數由大到小的順序是____.
(3)煙道氣中含有大量 CO2,經“捕捉”可用于生產尿素、甲醇等產品。
①尿素[CO(NH2)2]屬于化學肥料中的___肥
②下圖是用“捕捉”的CO2生產甲醇的微觀示意圖,請根據實際情況補充完整:___
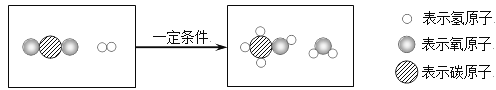
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】材料是時代進步的重要標志,有機合成材料的出現更是材料發展史上的一次重大突破。請回答下列問題:
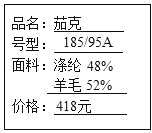
(1)由合成纖維與天然纖維混合紡織的面料,使衣眼穿起來既舒適又不易褶皺,如圖是某品牌服裝標簽上的部分內容,其中利用了合成纖維的_____________(填字母,下同)等優良性能。
A透氣性好 B彈性好 C耐磨 D吸水性強
(2)生活中常用________________的方法鑒別合成纖維和天然纖維。
(3)為了解決白色污染問題,禁止超市無償提供塑料購物袋,該舉措的意義是______________。
A節約資源 B保護生態環境 C增加超市的利潤 D倡導重復使用塑料袋
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】相同質量的下列物質①Zn②ZnO③Zn(OH)2④ZnCO3,分別跟質量分數都相同且適量的稀鹽酸充分反應,所得溶液的溶質質量分數的關系正確的是( )
A.①>②>③>④B.④>③>②>①C.①>②=④>③D.④>①>②=③
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】“細菌冶金”的原理是利用氧化鐵硫桿菌促使黃鐵礦(主要成分FeS2)氧化成硫酸鐵和硫酸,并為CO2和H2O合成有機物提供能量,流程如下圖。下列說法錯誤的是 ( )
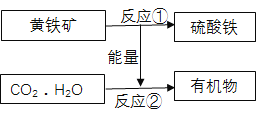
A. 氧化鐵硫桿菌在反應①中起催化作用
B. 整個流程提高了能量的利用率
C. 圖中有機物可能含碳、氫、氧元素
D. 反應①化學方程式:4FeS2+15O2+2X=2Fe2(SO4)3+2H2SO4,X為H2O2
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖是 A、B、C 三種物質的溶解度曲線。據圖回答下列問題。

(1)10℃時,B 物質的溶解度為___________,
(2)A 和 B 的交點 M 點的意義是:___________,
(3)如果 A 中混有少量的 C,可以采取__________方法提純 A。
(4)50℃時 A、B、C 飽和溶液降溫到 40℃時,溶質質量分數由小到大的順序_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】2015年11月,我國首架大型客機C919(如下圖)正式下線,實現了我國航空領域的新突破。回答下列問題:

(1)圖中標示的材料中,含有金屬元素的是 (寫出一種即可);屬于有機合成材料的是 。
(2)飛機大量使用合金材料,原因是 。
(3)鋁的金屬活動性比鐵的 (填“強”或“弱”)。空氣中,鋁比鐵具有更好的抗腐蝕性,原因是 (結合化學方程式解釋)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com