
【題目】碳是形成化合物種類最多的元素,含碳物質是中學化學研究的重要內容.
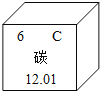
(1)如圖為元素周期表中的一格,下列說法不正確的是______.
A.碳元素屬于非金屬元素
B.碳原子核內質子數為6
C.碳元素的原子結構示意圖為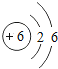
D.碳的相對原子質量為12.01
(2)“低碳生活”倡導低能耗、低污染、低排放,主要是為了減少______(填化學式)的排放量.下列做法符合“低碳經濟”的是______.
①提倡發送電子賀卡②大力發展火力發電③研制和開發新能源④提倡使用一次性木筷⑤增強室內自然采光
(3)二氧化碳和氨氣(NH3)在高溫、高壓下反應,生成尿素[CO(NH2)2]和水,反應的化學方程式是______.
【答案】C CO2 ①③⑤ CO2+2NH3![]() CO(NH2)2+H2O
CO(NH2)2+H2O
【解析】
(1)A、因碳的偏旁為“石”,則碳元素為非金屬元素,故A正確;B、由信息可知,碳原子的質子數為6,故B正確;C、碳原子的質子數為6,則原子結構中最外層電子數應為4,故C錯誤;D、由信息可知,碳原子的相對原子質量為12.01,故D正確;故選C.
(2)“低碳生活”倡導低能量、低消耗,主要是為了減少二氧化碳的排放,通過技術創新、制度創新、產業轉型、新能源開發等多種手段,盡可能地減少煤炭、石油等高碳能源消耗,減少溫室氣體排放,達到經濟、社會發展與生態環境保護雙贏的一種經濟發展形態,屬于低碳經濟.①提倡發送電子賀卡、③研制和開發新能源、⑤增強室內自然采光都可減少二氧化碳的排放,而②大力發展火力發電需要燃燒煤,增加二氧化碳的排放;④提倡使用一次性木筷必然要砍伐木材,減少了自然界對二氧化碳的吸收.
(3)二氧化碳和氨氣(NH3)在高溫、高壓下反應,生成尿素[CO(NH2)2]和水,反應的化學方程式是CO2+2NH3![]() CO(NH2)2+H2O.
CO(NH2)2+H2O.


科目:初中化學 來源: 題型:
【題目】如圖所示為實驗室中常見氣體制備、凈化、干燥、收集和進行實驗探究的部分儀器,某化學小組的同學欲利用其進行下列各化學實驗。根據題目要求,請回答下列問題:
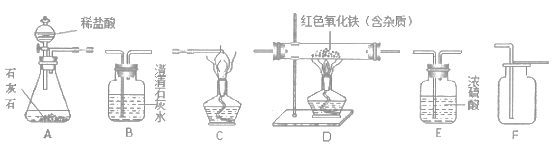
(1)在實驗室中制備并收集干燥的二氧化碳氣體。
①所選儀器的連接順序為:A→_____→_____(填寫儀器序號字母)。
②儀器A中,發生反應的化學方程式為_____。
③下列關于二氧化碳的敘述正確的是_____(填A、B、C、D之一)。
A.二氧化碳是一種有毒的氣體,屬于大氣污染物
B.二氧化碳通入紫色石蕊試液中,會觀察到紫色石蕊試液變藍
C.二氧化碳的固體俗名“干冰”,干冰易升華,可用于人工降雨
D.二氧化碳能滅火的根本原因是二氧化碳的密度比空氣大
(2)欲用一氧化碳氣體測定某不純氧化鐵樣品的純度(雜質不反應),并驗證反應中氣體生成物的性質。所選儀器的連接順序為:CO氣體→D→B→C。
①儀器B中看到的現象是_____。
②儀器C的作用是_____。
③寫出D中發生反應的化學方程式_____。
④反應前D中固體的總質量_____(填“大于”“小于”“等于”之一)反應后D中固體的總質量。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】取25g粉碎的石灰石樣品![]() 雜質不溶于水也不與鹽酸反應
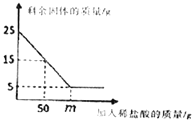
雜質不溶于水也不與鹽酸反應![]() ,放入小燒杯中,慢慢加入一定濃度的稀鹽酸,測得稀鹽酸的用量與固體的質量關系如圖所示。請回答下列問題:
,放入小燒杯中,慢慢加入一定濃度的稀鹽酸,測得稀鹽酸的用量與固體的質量關系如圖所示。請回答下列問題:
(1)上述實驗過程中發生反應的化學方程式為______。
(2)石灰石樣品中碳酸鈣的質量分數是______。
(3)根據已知條件列出反應所得氣體質量![]() 的比列式______。
的比列式______。
(4)圖中![]() ______。
______。
(5)![]() 稀鹽酸中含有HCl的質量為______g。
稀鹽酸中含有HCl的質量為______g。
(6)用100t此石灰石可制取含雜質![]() 的氧化鈣的質量為______。
的氧化鈣的質量為______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為測定黃銅(Cu﹣Zn合金)中銅的質量分數,某同學將20g該合金放入到盛有100g鹽酸的燒杯中,鋅與鹽酸恰好完全反應。反應停止后,測得燒杯中剩余物的總質量為119.8g。
(1)生成氫氣的質量為_____;
(2)計算合金中鋅的質量_____;(寫出計算過程)
(3)計算合金中銅的質量分數_____;(寫出計算過程,精確到0.1%);
(4)計算鹽酸中溶質的質量分數_____。(寫出計算過程,精確到0.1%)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列敘述中,符合質量守恒定律的是( )
A. 水結冰前后,質量保持不變
B. 36g水通電完全分解,可得到2g的氫氣
C. l00g過氧化氫溶液中,含有30g過氧化氫和70g水
D. 1.2g碳與3.2g氧氣反應可生成4.4g二氧化碳
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】碘是人體必需的微量元素之一。下圖是元素周期表中提供的碘元素的部分信息及碘原子的結構示意圖。下列說法錯誤的是
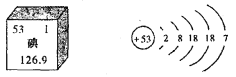
A.碘的相對原子質量為126.9,原子核內質子數為53
B.碘原子核外共有53個電子,最外層有7個電子
C.碘元素屬于非金屬元素,碘原子在化學反應中易得電子
D.碘鹽中含有碘酸鉀(KIO3),KIO3中碘元素的化合價為一1價
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】硫酸(H2SO4)是一種用途廣泛的化工原料,工業上常用煅燒黃鐵礦(主要成分是FeS2)的方法來生產硫酸,簡要的工藝流程圖如下:
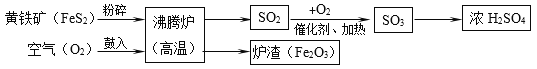
(1)黃鐵礦投入沸騰爐前粉碎的目的是________。
(2)在沸騰爐中發生的反應為:(______)FeS2+(______)O2 ![]() (______)Fe2O3+(______)SO2(請在化學式前面配上適當的化學計量數),得到的爐渣(Fe2O3)可用來煉鐵。
(______)Fe2O3+(______)SO2(請在化學式前面配上適當的化學計量數),得到的爐渣(Fe2O3)可用來煉鐵。
(3)請寫出流程中SO2轉化為SO3的化學方程式_________。
(爐渣的綜合利用)
為了實現爐渣(Fe2O3)的綜合利用,工業上把爐渣和焦炭、石灰石一起投入高爐,主要反應過程如圖:
![]()
(4)步驟②發生反應的化學方程式為______。
(5)下列有關高爐煉鐵的說法正確的是_______(填序號)。
A.上述流程中涉及的三個反應均為吸熱反應
B.上述步驟①反應中,還原劑是焦炭
C.焦炭的作用之一是為煉鐵爐提供高溫條件
D.焦炭的另一個作用是除去鐵礦石中的雜質
(6)分析高爐所得的生鐵中單質鐵的含量:
小瑾同學為測定生鐵中鐵的質量分數,先后進行了四次實驗,實驗數據記錄如下表。根據她的實驗數據,試計算生鐵中鐵的質量分數是_________?
第一次 | 第二次 | 第三次 | 第四次 | |
所取生鐵的質量∕g | 10 | 10 | 10 | 10 |
所加稀硫酸的質量∕g | 25 | 50 | 75 | 100 |
生成氫氣的質量∕g | 0.10 | 0.20 | 0.30 | 0.35 |
(反思質疑)
小宇同學在梳理工業煉鐵的相關知識時,提出了以下質疑:
(質疑一)焦炭也具有還原性而且成本低,工業煉鐵為什么不直接用焦炭作為還原劑冶煉鐵礦石?
(7)他設計了下圖所示的一組對比實驗:稱取兩份相同質量的氧化鐵粉末,一份與足量的焦炭粉末混合均勻放入裝置A的試管中,另一份放入裝置B的玻璃管中。
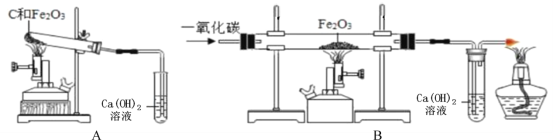
①裝置B的玻璃管中發生反應的化學方程式為________。
②當他觀察到裝置B的玻璃管中固體_________、澄清石灰水變渾濁時,裝置A
③通過上述實驗對比,小宇同學認為工業上不直接用焦炭作為還原劑煉鐵的主要原因有:反應不充分、反應速度慢、_______等。
(質疑二)裝置B中反應后的黑色固體一定就是單質鐵嗎?
(查閱資料)
a.鐵常見的氧化物有氧化鐵(Fe2O3)、四氧化三鐵(Fe3O4)和氧化亞鐵(FeO)。
b.四氧化三鐵是具有磁性的黑色晶體,氧化亞鐵是不溶于水的黑色粉末,無磁性,也不能被磁鐵吸引。
④小宇同學設計了如下實驗方案:用磁鐵吸引裝置B進行實驗后的黑色固體,發現黑色固體可以部分被吸引,由此得出結論:黑色固體的成分是___________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據下圖回答問題。
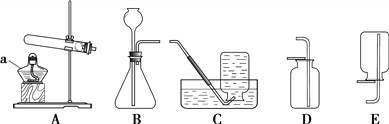
(1)儀器a的名稱是_____________。
(2)用高錳酸鉀制取氧氣的化學方程式為______________________________,用C裝置收集的氣體應具有的性質是______________________。
(3)用大理石和稀鹽酸制取二氧化碳時,所選用的發生裝置是___________,用D裝置收集二氧化碳的驗滿方法是_____________________________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】稀土有工業“黃金之稱”,我國稀土資源豐富。如圖是稀土元素錸在周期表中的信息,下列關于錸的信息錯誤的是![]()
![]()

A. 錸是金屬元素 B. 錸原子的質子數為75
C. 一個錸原子質量為![]() D. 錸的元素符號為Re
D. 錸的元素符號為Re
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com