
【題目】物質之間轉化(元素化合物),A~M均為初中化學常見物質,其中A是大理石主要成分;B是人體胃酸的一種主要成分;F是澄清石灰水主要成分;E是鈉鹽,其水溶液呈堿性;它們之間有如圖所示的相互轉換關系(圖中部分生成物已略去).
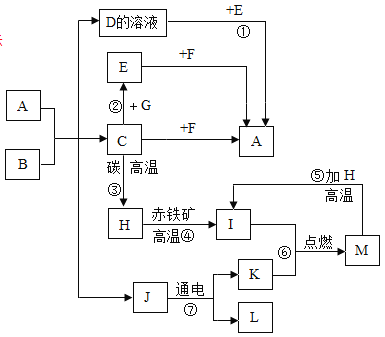
請回答下列問題:
(1)E的俗稱為_____(填其中一個)。
(2)寫出通電電解J時化學方程式_____,在電解的過程中通常加入少量燒堿或硫酸的目的是增強J物質的_____(填一物理性質)。
(3)實驗室進行有關反應④的實驗,當固體全部轉化為生成物時,固體顏色由_____色變為_____色。
(4)反應①-⑦中不涉及的基本反應類型是_____反應(填“化合”“分解”“置換”或“復分解”)。
(5)請寫出⑤的化學方程式_____。
(6)為了除去D溶液中少量的B物質,可向溶液中加入過量的_____(從A或F中選擇填入所加物質對應的英文序號),然后過濾,所得濾液即為純凈的D溶液。
【答案】純堿或蘇打 ![]() 導電性 紅 黑 置換
導電性 紅 黑 置換 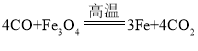 A
A
【解析】
由題干條件可知A為CaCO3,B為HCl,F是Ca(OH)2,A和B反應生成J能通電分解,則J為水,D為CaCl2,C為CO2,CO2與Ca(OH)2生成沉淀A CaCO3,CaCl2能與E反應生成CaCO3,E是鈉鹽,其水溶液呈堿性,故E為Na2CO3,CO2能與氫氧化鈉溶液反應生成碳酸鈉,則G為氫氧化鈉,CO2能與碳在高溫條件下生成CO,則H為CO,CO可以與氧化鐵高溫條件下反應生成Fe和二氧化碳,則I為Fe,Fe能與氧氣反應生成Fe3O4,M是Fe3O4,電解水生成氫氣和氧氣,則K是O2,L是H2。
(1)E是碳酸鈉,俗稱是純堿或蘇打。
(2)電解水生成氫氣和氧氣,化學方程式為![]() ;在電解的過程中通常加入少量燒堿或硫酸的目的是增強水的導電性。
;在電解的過程中通常加入少量燒堿或硫酸的目的是增強水的導電性。
(3)實驗室進行一氧化碳高溫下還原氧化鐵實驗時,生成鐵和二氧化碳,固體粉末由紅色變為黑色。
(4)由題中轉化關系可知:①為復分解反應;②不屬于四大基本反應;③為化合反應;④為還原反應,不屬于四大基本反應;⑤為還原反應,不屬于四大基本反應;⑥為化合反應;⑦為分解反應,故①~⑦中不涉及四大基本反應中的置換反應;
(5)反應⑤為一氧化碳和四氧化三鐵高溫條件下生成鐵和二氧化碳,反應的化學方程式為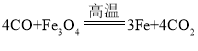 ;
;
(6)除去CaCl2溶液中含少量HCl,可加入過量的A(CaCO3),碳酸鈣與鹽酸反應生成氯化鈣、二氧化碳和水,過量的CaCO3過濾即可除去。


 應用題作業本系列答案
應用題作業本系列答案科目:初中化學 來源: 題型:
【題目】以甲為原料合成化工產品丁的微觀過程如下圖,下列說法正確的是
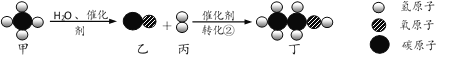
A. 轉化①屬于置換反應B. 轉化②中乙和丙的分子個數之比為1∶3
C. 一定濃度的丁溶液可作消毒劑D. 轉化過程中元素化合價無變化
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請回答下列有關燃燒的問題:
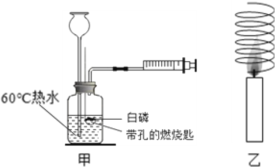
(1)用如圖甲所示裝置,熱水中的白磷不燃燒,但當用注射器向瓶內推入空氣,瓶內水面下降,當白磷露出水面時立即燃燒,說明可燃物燃燒的條件是_______,白磷燃燒的化學方程式為________________。
(2)如圖乙將一根銅絲燒成螺旋狀網罩罩在一支燃著蠟燭的火焰處,不多久蠟燭火焰熄滅,其熄滅的原因是___________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】水是人類寶貴的自然資源,我們應該了解有關水的知識。
(1)有一種家用環保型消毒液發生器,其中發生的主要反應是氯化鈉和水在通電條件下反應生成氫氧化鈉、氫氣和氯氣(Cl2),該反應的化學方程式為_____。
(2)溶液在生產和生活中有著廣泛的應用。某同學配制溶液時,在用量筒量取水的過程中俯視讀數,這樣配制得到的溶液的溶質質量分數會_____(填“偏大”“偏小”或“無影響”)。
(3)A1與NaOH溶液反應會生成NaA1O2和H2,該反應的化學方程式為_____;已知化學反應前后元素化合價發生改變的屬于氧化還原反應,反應物中,元素化合價升高被氧化是還原劑,化合價降低被還原是氧化劑,則該反應中H2O是_____(填氧化劑,還原劑)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】乙烯(C2H4)是一種催熟水果的激素。一定質量的乙烯在不充足的氧氣中燃燒,生成物只有CO、CO2和H2O,且總質量為120g,其中H2O 36g,則CO的質量為_____;該反應的化學方程式為_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲、乙兩固體物質的溶解度曲線如圖所示,下列說法正確的是( )
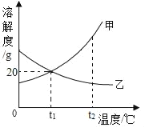
A. t1℃時,甲乙的溶解度相等,它們飽和溶液的溶質質量分數也相等,都為20%
B. t1℃時,30g甲加入到50g水中最多可得80g溶液
C. t2℃,甲、乙兩物質的飽和溶液分別降溫到t1℃時,所得溶液中溶質質量分數的大小關系是:甲>乙
D. t2℃,等質量的甲、乙兩物質的飽和溶液分別降溫到t1℃時,所得溶液質量的大小關系為:甲>乙
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】硒元素在有機體的生命活動過程中具有重要的生物學作用,是人體必需的15種每日膳食營養元素之一,硒缺乏與人類許多疾病的發生有密切關系。同時硒元素過多也可以引起毒性作用。如圖為硒在元素周期中的信息,下列所獲取的信息中錯誤的是( )
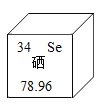
A.硒的核電荷數為34B.硒的元素符號為Se
C.硒是一種金屬元素D.硒的相對原子質量為78.96
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】人體胃液中含有的酸是_______________。右圖是沾有污漬的某抗酸的部分說明,同學們對此展開了系列研究。

Ⅰ.服用方法探究:為什么嚼碎后服用?你認為需后服用的自的是____________。
Ⅱ.抗酸原理探究:
(1)含有NaHCO3相Al(OH)3的藥片都能用于治療胃酸過多,反應原理用方程式可表示為(任寫一個)_______________。
(2)查閱資料可知鋁碳酸鎂是層狀結構(如圖),則鋁碳酸鎂中起到抗酸作用的微粒的符號有____。
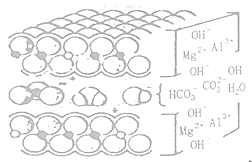
Ⅲ.主成分探究:
(查閱資料)鋁碳酸鎂片加感分解的產物為Al2O3、MgO、CO2和H2O,藥品中的其它成分受不分解。
(實驗過程)學習小設計了如下圖的實驗探究鋁碳酸鎂片的組成。

(1)檢查裝置氣密性,取8.6g該藥片,研成粉末放入硬質玻璃管中;
(2)實驗開始前先通入一定量空氣,然后稱量裝置D的質量;
(3)點燃消精燈加熱。充分反應后,停讓加熱;
(4)通入空氣至玻璃管冷卻,目的是防止液體倒吸和___________,然后測得裝置D增重0.44g。
(實驗結論)鋁碳酸鎂的化學式為____________。藥片中鋁碳酸鎂的質量分數是________。
(拓展延伸)有醫生生建議患有嚴重胃脹、胃潰瘍的患者最好慎用該藥而改服氫氧化鋁片,試用你學的知識解釋這樣建議的理由是_____________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請按照要求完成下列金屬性質的探究:
探究一:鋁片與鹽酸反應過程中的能量及反應速率的變化。
(1)實驗時需將鋁片進行打磨,其目的是_____。
(2)反應中試管外壁發燙,說明鋁與鹽酸反應是_____(填“吸熱”或“放熱”)反應,化學方程式為_____。
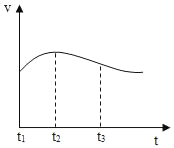
(3)實驗測得鋁片產生氣體的速率(v)與時間(t)的關系如圖所示,t1~t2時間內反應逐漸加快的主要原因是_____。
(查閱資料)鐵、銅均能與氯化鐵溶液反應,化學方程式分別為:2FeC13+Fe═3FeCl2、2FeCl3+Cu=2FeCl2+CuCl2
(4)向氯化鐵和氯化銅的混合溶液中,加入一定量的鐵粉,充分反應后過濾。取少量濾渣加入稀鹽酸,有氣泡產生。則濾液中的溶質是_____,濾渣中一定含有_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com