
【題目】如圖是氫氧化鈉溶液與稀鹽酸恰好完全反應的微觀示意圖,下列結論錯誤的是( )
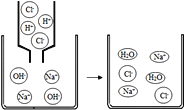
A. 反應結束時溶液的pH=7
B. 反應前后元素的種類沒有變化
C. 反應后溶液中存在的粒子只有Na+和Cl﹣
D. 該反應的實質是H+和OH﹣結合生成水
科目:初中化學 來源: 題型:
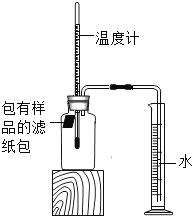
【題目】小明對鐵的銹蝕進行如下探究,室溫時,將包有樣品的濾紙包用大頭針固定在橡膠塞上,迅速塞緊,裝置如圖,觀察到量筒內水沿導管慢慢進入廣口瓶(凈容積為146mL)。當溫度恢復至室溫,且量筒內水面高度不變時讀數(此時瓶內氧氣含量近似為零)。記錄起始和最終量筒的讀數以及所需時間如表。
序號 | 樣品 | 量筒起始 讀數/mL | 量筒最終 讀數/mL | 所需時間 /min |
1 | 1g鐵粉、0.2g碳和10滴水 | 100 | 70 | 約120 |
2 | lg鐵粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 約70 |
3 | …… | 100 | 70 | 約480 |
(1)實驗①和②說明NaCl可以_____鐵銹蝕的速率。
(2)實驗開始后,廣口瓶內溫度有所上升,說明鐵的銹蝕過程是_____(填“放熱”或“吸熱”)過程。
(3)實驗結束后取出濾紙包,觀察到有紅棕色物質生成,該物質的化學式是_____。
(4)已知含碳能夠加快鐵的生銹速度,小明想通過實驗①和③是探究碳對鐵銹蝕速率的影響,請在表格空白處填寫實驗③的樣品組成_____。
(5)該裝置還可用于測量空氣中氧氣的含量,根據上述數據計算氧氣的體積含量是_____(小數點后保留1位)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據所學知識并結合下列儀器,回答有關問題
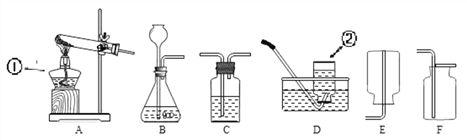
(1)寫出對應儀器的名稱:①_________________ ②___________________。
(2)實驗室加熱高錳酸鉀制取并收集一瓶較純凈的氧氣,應選擇的裝置組合是_____(填序號),該反應的化學方程式______;若收集的氧氣不純,其可能原因有________(填一種即可)。
(3)常見氣體發生裝置除了固體加熱型和固液不加熱型之外,還有固液加熱型等。下圖G裝置是用銅和濃硫酸反應的實驗裝置
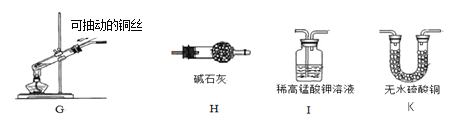
①反應原理:Cu + 2H2SO4(濃) △______+ SO2↑ + 2H2O
②G裝置中將銅絲設計為可抽動,是為了控制___________________。
③生成物中的SO2是一種空氣污染物,它會導致_____________(填一種空氣污染名稱)。
④若要驗證生成物中有SO2和水蒸氣,請從H、I、K中選擇合適的裝置序號填空:G →____→___________→尾氣處理裝置。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據所給的信息和標志,判斷下列說法錯誤的是
A | B | C | D |
《淮南萬畢術》中記載,曾青得鐵則化為銅。 | 《夢溪筆談》中記載,鄜、延境內有石油,舊說“高奴縣出脂水”,即此也。 |
|
|
是現代濕法冶金的先驅 | 這里的石油指的是一種油脂 | 看到有該標志的丟棄物,應遠離并報警 | 貼有該標志的物品是可回收物 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為測定標有質量分數為32%的鹽酸的實際質量分數,小明實驗時先在燒杯中加入20 g 40%的氫氧化鈉溶液,再逐滴加入該鹽酸,測定出加入鹽酸的質量與燒杯中溶液pH的關系如圖。
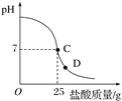
(1)所用氫氧化鈉溶液中溶質的質量為_____g。
(2)請認真看清上圖信息后回答以下問題。
①當滴加鹽酸到C點時,所消耗的鹽酸中溶質的質量是多少?_____。
②該鹽酸的實際質量分數是多少?(保留到0.1%)_____。
③導致鹽酸溶液的溶質質量分數改變的原因是_____。
④當滴加鹽酸到圖像中D點時,燒杯中溶液的溶質是_____(填化學式)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖是某化學興趣小組。設計的金屬活動性順序的探究實驗。
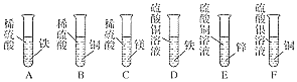
(1)上述實驗中,有氣泡生成的是________(填寫裝置序號)。
(2)試管F中出現的實驗現象是______________。
(3)上述實驗能否證明鎂、鋅、鐵、銅、銀五種金屬的活動性強弱?____請說明理由_____。
(4)我國古代“濕法煉銅”就是利用了試管D中的反應原理,請寫出該反應的化學方程式:______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(10分)南海、釣魚島及其附屬海域是我國固有領土,蘊藏著豐富的海洋資源。
(1)海水制鹽。從海水制取的粗鹽中含有泥沙、硫酸鎂和氯化鈣等雜質,為得到較純的氯化鈉,將粗鹽溶于水,然后進行如下操作:a.加過量的Ba(OH)2溶液;b.加稍過量的鹽酸;c.加過量的Na2CO3溶液;d.過濾;e.蒸發。正確的操作順序是 (填字母)。加Na2CO3溶液的作用是除去 。
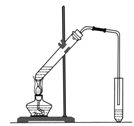
(2)海水淡化。下圖是一個簡易的蒸餾法淡化海水的裝置。證明得到的水是淡水的方法是 。
(3)海水制鎂。從海水中提取金屬鎂的過程如下圖所示:
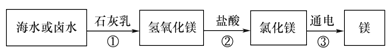
在上述轉化過程中發生中和反應的是 (填反應順序號)。海水中本身就含有氯化鎂,則①、②兩步的作用是 。
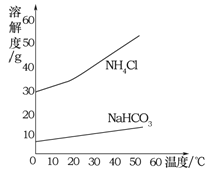
(4)海水“制堿”。氨堿法制純堿是先通過化學反應生成NaHCO3和NH4Cl,NaHCO3結晶析出,再加熱NaHCO3制得純堿。
①氨堿法制純堿中生成NaHCO3和NH4Cl的化學方程式為 ;
②反應中生成NaHCO3和NH4Cl的質量比為84∶53.5,NaHCO3和NH4Cl的溶解度曲線如圖所示。請分析NaHCO3結晶析出而NH4Cl沒有結晶析出的原因是 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲、乙、丙、X、Y、Z六種初中常見的物質,甲、乙、丙含有相同的金屬元素,甲常作為補鈣劑;X的固體常用于人工降雨,Y、Z都顯堿性,但不屬于同類別物質,Z俗稱為純堿。(“﹣”表示物質之間發生反應,“→”表示物質之間能一步轉化)回答下列問題:
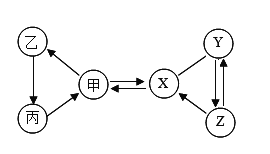
(1)Z的化學式為_____。
(2)寫出乙→丙反應的化學方程式:_____,反應類型為_____(填基本反應類型),該反應過程中_____(填“放熱”或“吸熱”)
(3)①寫出X+Y反應的化學方程式:_____。②寫出Z→Y的反應的化學方程式:_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某純堿樣品中含有少量NaCl,小麗同學取該樣品23g全部溶解于150g水中,再逐滴加入160g稀鹽酸,反應中產生的氣體的質量與鹽酸的用量關系如圖所示。(提示:相關反應為Na2CO3+2HCl=2NaCl+H2O+CO2↑)計算當恰好完全反應時:
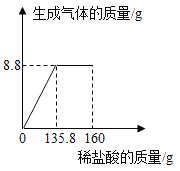
(1)產生的二氧化碳的質量是 克。
(2)此時所得到的溶液中溶質的質量分數(寫出必要的計算過程,結果保留到0.1%)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com