
【題目】【改編】(8分)常溫下沒有氧氣存在時,鐵與水幾乎不反應,但高溫下,鐵與水蒸氣能反應生成一種常見鐵的氧化物和一種氣體。小明很好奇,設計如下實驗探究鐵粉與水蒸氣反應后的產物。
(1)探究生成的氣體是什么?
用燃著的木條靠近肥皂泡,有爆鳴聲,稍后有肥皂泡飄到空中。說明生成的氣體是________。
(2)探究試管中剩余固體成分是什么?
【查閱資料】
常見鐵的氧化物 | FeO | Fe2O3 | Fe3O4 |
顏色、狀態 | 黑色粉末 | 紅棕色粉末 | 黑色晶體 |
能否被磁鐵吸引 | 否 | 否 | 能 |
Fe3O4+8HCl= FeCl2+2FeCl3+4H2O
【初步驗證】試管中剩余固體為黑色,能全部被磁鐵吸引,那么該黑色固體不可能含有_______(化學式),
【猜想與假設】猜想一:剩余固體是Fe與Fe3O4;猜想二:剩余固體是_____________。
【實驗探究】
實驗操作 | 實驗現象及結論 |
【實驗結論】鐵和水蒸氣反應的化學方程式為___________________________________(2分)。
【反思與交流】初中我們還學過通過_______________________________(化學方程式)得到Fe3O4。
【答案】(1)H2 ;(2)【初步驗證】Fe2O3和FeO(寫全才有分)【猜想與假設】猜想二:剩余固體全是Fe3O4
【實驗探究】
實驗操作 | 實驗現象及結論 |
取少量黑色固體于試管中,加入足量的稀鹽酸。 | 若固體全部溶解,沒有氣泡冒出,剩余固體是Fe3O4,若固體全部溶解,有氣泡冒出,剩余固體是Fe與Fe3O4 |
【實驗結論】3Fe+4H2O高溫Fe3O4+4H2↑
【反思與交流】3Fe+2O2![]() Fe3O4
Fe3O4
【解析】
試題分析:(1)根據質量守恒定律,又該氣體密度比空氣小還具有可燃性,那么只能是氫氣;
(2)【初步驗證】根據資料固體為很少排出紅棕色的Fe2O3,又能全被磁鐵吸引能同時排除Fe2O3和FeO;
【猜想與假設】剩余固體已經說明是鐵能與水反應生成鐵的氧化物,該氧化物為Fe3O4,那么固體成分就只需要考慮鐵這一變量了,鐵是否被完全消耗即有無鐵,結合猜想一故猜想二:剩余固體只有Fe3O4
【實驗探究】酸的化學性質:能與活潑金屬反應生成氫氣,同時還能與金屬氧化物反應,故可設計實驗
實驗操作 | 實驗現象及結論 |
取少量黑色固體于試管中,加入足量的稀鹽酸。 | 若固體全部溶解,沒有氣泡冒出,剩余固體是Fe3O4。(1分)若固體全部溶解,有氣泡冒出,剩余固體是Fe與Fe3O4 |
【實驗結論】根據信息:高溫下,鐵與水蒸氣能反應生成一種常見鐵的氧化物和一種氣體,故反應的化學方程式為:3Fe+4H2O高溫Fe3O4+4H2↑
【反思與交流】能生成Fe3O4,就是鐵在氧氣中燃燒了。


科目:初中化學 來源: 題型:
【題目】無色透明普通玻璃,其主要成分又稱為鈉鈣玻璃(化學式為Na2CaSi6O14),其中硅元素的化合價為
A、+4價 B、+3價 C、+2價 D、+1價
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(4分)認真分析下列各圖,回答相關問題:

(1)根據圖1分析,20℃時,將20g NaCl加入50g水中形成溶液的質量為____________。
(2)圖2中打開汽水瓶冒出大量氣泡,說明氣體的溶解度與____________有關。
(3)在圖3所示的燒杯中加入一定量的硝酸銨,溶解后甲試管內出現的現象是______________;乙試管內的溶液是____________(填“飽和”或“不飽和”)溶液。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】分類是學習化學的方法之一。下列各組物質是按單質、氧化物、混合物的順序排列的是
A.氧氣、冰水混合物、空氣 B.氮氣、氯酸鉀、白酒
C.水銀、二氧化硫、冰水混合物 D.紅磷、高錳酸鉀、食醋
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某物質的分子模型示意圖為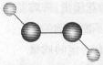 ,其中“
,其中“![]() ”代表氫原子,“
”代表氫原子,“![]() ”代表氧原子,下列敘述正確的是
”代表氧原子,下列敘述正確的是
A.此物質屬于混合物 B.此物質的化學式為HO
C.此物質中含有氧分子 D.此物質的一個分子由4個原子構成
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列四組物質中,均屬于氧化物的是
A.氧氣、氧化鈣、四氧化三鐵 B.水、二氧化硫、高錳酸鉀
C.空氣、氧化銅、五氧化二磷 D.過氧化氫、氧化鎂、二氧化碳
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com