
【題目】小軍同學在實驗室幫老師整理藥品時發現NaOH溶液試劑瓶口有一些白色固體,于是生好奇心:這白色固體是什么?他為此進行了如下探究
(查閱資料)①NaOH在空氣中變質不會生成NaHCO3;
②CO2不溶解于飽和NaHCO3溶液中,也不與NaHCO3反應;
③Fe(OH)3呈紅褐色,難溶于水;BaCl2溶液呈中性。
(提出猜想)猜想一:是NaOH
猜想二:是Na2CO3
猜想三:_____
(實驗探究)小軍進行了下列實驗探究
實驗操作 | 實驗現象 | 實驗結論 |
①取少量白色固體于試管中,加水溶解,再加入足量BaCl2溶液 | _____ | 猜想二正確 |
②過濾,在濾液中加入FeCl3溶液 | 無紅褐色沉淀生成 |
(問題分析)實驗操作①中加入足量BaCl2溶液的作用是_____,實驗操作②還有其他實驗方案嗎?如有,請寫出一種實驗方案(必須指明試劑和現象)_____。為了提高實驗結論的準確性,小軍又設計了如圖所示的實驗對該白色固體的性質進行進一步探究:
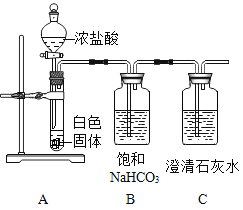
(實驗現象)A中有大量氣泡產生,C中實驗現象是_____
(實驗結論)白色固體是Na2CO3
(分析與反思)小軍在與老師進行交流后得知,自己所設計的實驗存在一定的缺陷,他對自己實驗中存在的問題進行了反思:裝置B中也能產生CO2。寫出裝置B中產生CO2的化學反應方程式_____。改進措施:_____。
【答案】是NaOH和Na2CO3混合物 產生白色沉淀 檢驗并且除去碳酸鈉,防止它對氫氧化鈉檢驗產生干擾 過濾,在濾液中滴加酚酞試液,溶液變紅色,說明溶液中含有氫氧化鈉 澄清石灰水變渾濁 NaHCO3+HCl═NaCl+H2O+CO2↑ 濃鹽酸換為稀鹽酸
【解析】
提出猜想:
猜想一:氫氧化鈉沒有變質:是NaOH 猜想二:氫氧化鈉全部變質:是Na2CO3 猜想三:氫氧化鈉部分變質:是NaOH、Na2CO3。
實驗探究:
①取少量白色固體于試管中,加水溶解,再加入足量BaCl2溶液,產生白色沉淀,是因為氯化鋇和碳酸鈉反應生成了碳酸鋇沉淀和氯化鈉;
②對上述操作后的濾液進行過濾,在濾液中加入FeCl3溶液,無紅褐色沉淀生成,說明溶液中不含有氫氧化鈉。
猜想二正確。
問題
實驗操作①中加入足量BaCl2溶液的作用是檢驗并且除去碳酸鈉,防止它對氫氧化鈉檢驗產生干擾;
實驗操作②的主要目的是驗證溶液中是否有氫氧化鈉,可以通過驗證溶液中是否存在氫氧根來驗證。故有其他方案,如:過濾,在濾液中滴加酚酞試液,溶液變紅色,說明溶液中含有氫氧化鈉(合理即可)。
實驗現象:
氯化氫和碳酸氫鈉反應生成氯化鈉、水和二氧化碳,A中有大量氣泡產生,說明白色物質中含有碳酸鈉。二氧化碳能使澄清石灰水變渾濁,所以C中的實驗現象是澄清石灰水變渾濁。
分析與反思:
裝置B中也能產生CO2,是因為濃鹽酸具有揮發性,濃鹽酸揮發出的氯化氫在裝置B中和碳酸氫鈉反應生成氯化鈉、水和二氧化碳,反應的化學反應方程式:NaHCO3+HCl═NaCl+H2O+CO2↑。改進措施:將濃鹽酸換為稀鹽酸。


 一線名師口算應用題天天練一本全系列答案
一線名師口算應用題天天練一本全系列答案 小學學習好幫手系列答案
小學學習好幫手系列答案科目:初中化學 來源: 題型:
【題目】A、B在常溫下是液體,A與黑色固體物質甲混合可產生能使帶火星的木條復燃的氣體C和B,白色固體D與黑色固體甲在加熱的條件下也能生成C,同時得到白色固體E,紫黑色固體H加熱可得到C和甲及另一種物質F,紅色固體G在C中燃燒產生大量白煙,回答:
(1)F的化學式_____。
(2)寫出下列反應的文字表達式:D生成C的反應_____,G在C中燃燒_____。
(3)A轉化成B的反應類型是_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】能源利用和環境保護問題一直受到社會高度關注。
(1)從環境保護的角度考慮,最理想的燃料是_________(填化學式),它屬于________(填“可再生能源”或“不可再生能源”)。
(2)CNG( Compressed Natural Gas)汽車是指以壓縮天然氣替代常規汽油或柴油作為燃料的汽車。天然氣的主要成分是_______(填化學式),其是最簡單的____________(填“有機物”或“無機物”),天然氣燃燒的化學反應方程式___________________,主要是將化學能轉化為________能。
(3)中國政府決定2018年1月1日起全面禁止“洋垃圾”入境,大量垃圾對我國大氣、地表水、土壤等造成嚴重污染。
①“洋垃圾”中的廢五金含有多種金屬。攝入下列金屬不會造成中毒的是___________(填字母序號)。
a鉛 b鐵 c汞
②無用“洋垃圾”直接露天焚燒會產生許多有毒氣體,其中_________(填化學式)極易與血液中血紅蛋白結合,引起中毒。
(4)煤的燃燒會產生___________(寫化學式),形成“硫酸”型酸雨。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】向盛有50mL稀硫酸的燒杯中,緩慢滴加一定溶質質量分數的氫氧化鋇溶液至過量。隨著氫氧化鋇溶液的滴加,某些量變化趨勢正確的( )
A.  B.
B. 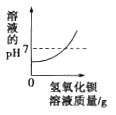 C.
C. 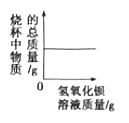 D.
D. 
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】將1.17g氯化鈉固體放入燒杯中,加入51.7g水充分溶解后得到常溫下氯化鈉的不飽和溶液,再向所得溶液中逐滴滴入100g一定溶質質量分數的硝酸銀溶液。實驗過程中生成沉淀的質量與滴入硝酸銀溶液的質量關系如圖所示:
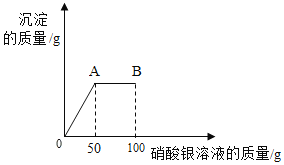
(1)B點時,溶液中所含硝酸銀的質量為______。
(2)A點時,所得溶液中溶質質量分數為____。(計算結果精確到0.1%)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在飽和的碳酸鈉溶液中通入CO2可用來制備碳酸氫鈉(NaHCO3),發生反應的化學方程式為Na2CO3+CO2+H2O = 2NaHCO3。由于溶解度不同,飽和碳酸鈉溶液中通入CO2會析出碳酸氫鈉晶體而使溶液變渾濁。某化學課外小組同學發現不同條件下出現渾濁的時間不同。
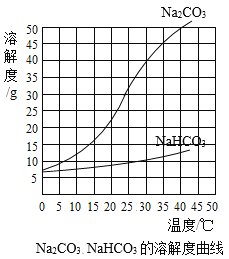
Na2CO3、NaHCO3的溶解度曲線
(提出問題)影響碳酸氫鈉晶體產生速率的因素有哪些?
(猜想與假設)碳酸氫鈉晶體產生速率的影響因素有溫度、試管內徑、CO2流速、飽和碳酸鈉溶液的體積。
(進行實驗)實驗裝置如下圖所示。每次實驗時均在試管里加入1mL飽和碳酸鈉溶液并在試管后放置一張寫有黑色字跡的白紙,從垂直于試管的方向觀察白紙上字跡的清晰程度,記錄時間,用于判斷碳酸氫鈉晶體的產生速率。部分實驗記錄如下表所示。
序號 | 溫度 | 試管內徑 | CO2流速 (個/秒) | 產生不同現象的時間 | ||
字跡變淡 | 字跡模糊 | 字跡消失 | ||||
① | 25 | 10 mm | 5-8 | 517" | 719" | 817" |
② | 32 | 10 mm | 5-8 | 350" | 409" | 428" |
③ | 40 | 10 mm | 5-8 | 348" | 406" | 418" |
④ | 25 | 14 mm | 5-8 | 636" | 738" | 828" |
⑤ | 25 | 25 mm | 5-8 | X | 943" | 1022" |
⑥ | 25 | 10 mm | 10-13 | 502" | 640" | 758" |
⑦ | 25 | 10 mm | 2-5 | 540" | 1045" | 1236" |
(解釋與結論)
(1)由上述溶解度曲線圖可獲得的信息有________(寫出一條即可)。
(2)錐形瓶中是利用碳酸氫鈉與稀硫酸(H2SO4)反應來制二氧化碳。除生成二氧化碳外,還有水和硫酸鈉(Na2SO4)生成,該反應的化學方程式為________。
(3)實驗①④⑤研究的影響因素是________。
(4)表中X應該是________。
A 605" B 845" C 955"
(5)通過對數據的觀察和分析,小明認為“二氧化碳流速越快,碳酸氫鈉晶體產生速率越快”,得到該結論的依據是________(填實驗序號)。
(6)結合實驗①②③,可得出的結論是_________。
(7)若要研究飽和碳酸鈉溶液的體積對碳酸氫鈉晶體產生速率是否有影響,需要控制的變量有________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】A、B、C、D、E、F、G、H都是第一、二單元里見過的物質,它們之間有如下的轉化關系。已知A為暗紫色固體,E、F常溫下為液體,B為能支持燃燒的無色氣體,D為二氧化錳。請回答下列問題:
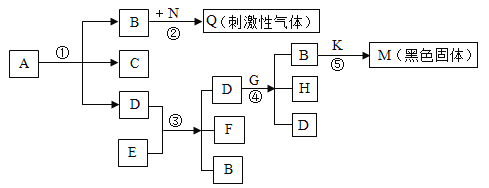
(1)寫出下列物質的名稱:B__________________;Q__________________。
(2)寫出下列反應的文字表達式:
①______________________;
④_____________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請在橫線上用恰當的化學用語表示。
(1)兩個銨根離子________;
(2)保持酒精化學性質的最小粒子_________;
(3)畫出硫酸鎂中的陽離子的結構示意圖________;
(4)天然氣主要成分________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】已知,A~E物質之間存在如圖轉化關系。其中A、C、D是單質,E是相對分子質量最小的氧化物,B為藍色溶液。
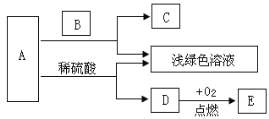
(1)寫出E物質的化學式:_____。
(2)淺綠色溶液中一定含有的金屬離子是_____。
(3)A→D的基本反應類型為_____。
(4)A和B反應的化學方程式為_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com