
【題目】元素周期表是學習和研究化學的重要工具.回答下列問題:
(1)元素周期表中不同元素間最本質的區別是 (填字母).
A.質子數不同 B.中子數不同 C.相對原子質量不同
(2)1869年, (填字母)發現了元素周期律并編制出元素周期表.
A.張青蓮 B.門捷列夫 C.拉瓦錫
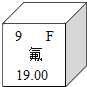
(3)元素周期表中氟元素的有關信息如圖所示,下列說法正確的是 (填字母).
A.氟屬于金屬元素 B.氟的原子序數是9 C.氟的相對原子質量是19.00g
(4)氟原子結構示意圖為![]() ,氟原子在化學反應中易 (填“得到”或“失去”)電子,由鈉元素和氟元素組成的化合物氟化鈉的化學式為 .
,氟原子在化學反應中易 (填“得到”或“失去”)電子,由鈉元素和氟元素組成的化合物氟化鈉的化學式為 .
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
【題目】工業鐵紅的主要成分是Fe2O3,還含有少量的FeO、Fe3O4.為了測定鐵紅中鐵元素的質量分數,興趣小組的同學進行了如下實驗,請你參與過程分析.
[資料1]堿石灰既能吸收水又能吸收二氧化碳;濃硫酸可以吸收水蒸氣;
[資料2]實驗室常用氫氧化鈉溶液來除去CO2 反應生成碳酸鈉和水;用澄清的石灰水
來檢驗CO2氣體;
[資料3]草酸晶體(H2C2O43H2O)在濃H2SO4作用下受熱分解,化學方程式為:
H2C2O43H2O![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
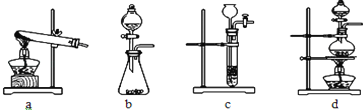
(1)下列可用作草酸分解制取氣體的裝置是 (填字母編號).
【問題討論】用下圖所示裝置進行實驗:
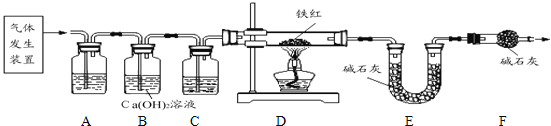
(2)實驗前應先 .
(3)進入D中的氣體是純凈、干燥的CO,則A、C中的試劑依次是 、 (填字母編號).
a.濃硫酸 b.澄清的石灰水 c.氫氧化鈉溶液
(4)寫出A裝置中發生的化學反應方程式 .
(5)B裝置的作用是 .
(6)對D裝置加熱前和停止加熱后,都要通入過量的CO,其作用分別是:
①加熱前 . ②停止加熱后 .
(7)寫出D裝置中所發生反應的一個化學方程式 .
【數據分析與計算】
[資料4]鐵的常見氧化物中鐵的質量分數:
鐵的氧化物 FeO Fe2O3 Fe3O4
鐵的質量分數 77.8% 70.0% 72.4%
(8)稱取鐵紅樣品10.0g,用上述裝置進行實驗,測定鐵紅中鐵的質量分數.
①D中充分反應后得到Fe粉的質量為m g,則 <m< .
②實驗前后稱得E裝置增重6.6g,則此鐵紅中鐵的質量分數是 .
【實驗評價】
反思1:本實驗中如果缺少C裝置(不考慮其它因素),則測得樣品中鐵的質量分數會 (填“偏小”、“不變”或“偏大”).
反思2:請指出【問題討論】中實驗裝置的一個明顯缺陷 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請從下列物質中選擇填空(填字母編號):
A.金剛石 B.碳酸鉀 C.二氧化硫 D.葡萄糖
(1)能形成酸雨的是 ;
(2)草木灰的主要成分是 ;
(3)“低血糖”的糖是 ;
(4)自然界中最堅硬的物質是 ;
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在一密閉容器中加入甲、乙、丙、丁四種物質,在運動條件下發生化學反應,測得反應前及t1、t2時各物質質量如圖所示,下列說法中不正確的是

A. 該反應為化合反應
B. 丙可能為該反應的催化劑
C. 該反應中,乙、丁的質量變化之比為7:5
D. 該反應中,甲、乙的質量變化之比為1:4
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某同學為了探究物質的性質,以氧氣為例,做了如下實驗:如圖所示,先收集了兩瓶氧氣后正放在桌上,蓋好玻璃片,然后用帶火星的木條插入A集氣瓶中,在B瓶中放入一只昆蟲.請回答下列問題.
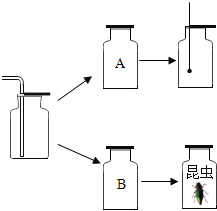
(1)觀察到的實驗現象:
A瓶 ;
B瓶 ;
(2)探究得出氧氣的部分性質:
物理性質 ;
化學性質 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】鋼鐵在生產、生活中有廣泛的用途.建造上海世博會的中國館﹣﹣“東方之冠”的核心筒就是用四根巨型鋼筋混凝土制成的,其中用了大量的鋼鐵.
(1)鋼鐵屬于 (填“純凈物”或“混合物”);
(2)煉鐵廠常以焦炭、赤鐵礦(主要成分是氧化鐵Fe2O3)、空氣等為主要原料煉鐵,請寫出一氧化碳與氧化鐵在高溫下反應的化學方程式: ;
(3)每年世界上鋼鐵的產量很高,鋼鐵的銹蝕也給人類帶來了巨大的損失.鐵在空氣中銹蝕,實際上是鐵跟空氣中的氧氣和 共同作用的結果.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】閱讀下面科普短文。
“瘋狂”的星球

金星是太陽系中八大行星之一,中國古代稱之為長庚、啟明、太白金星。金星地表大氣壓約是地球的90倍,大氣成分主要由二氧化碳組成,約占96%,因此它的地表具有強烈的溫室效應,在近赤道的低地,溫度可高達500°C。
在高度50至70公里的金星上空,懸浮著濃密的厚云,把大氣分割為上下兩層。你知道嗎?地球云層的主要成分是水(水的液滴),而金星云層的主要成分是硫酸(硫酸的液滴),其中還摻雜著硫的粒子,所以呈現黃色。H2SO4的生成主要源于太陽光中波長短于160nm的紫外光對CO2的光解,使其變為CO和原子氧,原子氧非常活潑,能與SO2反應變為SO3,SO3與水反應變為H2SO4,在金星,下的雨真是名副其實的酸雨。金星里,H2SO4的形成過程是不斷循環的,H2SO4從大氣較高較冷的區域降至較低較熱的區域,當溫度達到300℃時,H2SO4開始分解為SO3和水,SO3再分解為SO2和原子氧,原子氧接著與CO反應變為CO2。SO2與水會上升到上層,重新反應又釋放出H2SO4。
依據文章內容,回答下列問題。
(1)金星地表具有強烈的溫室效應是因為____________。
(2)原子氧的符號為____________。
(3)硫酸分解反應的化學方程式為____________。
(4)在硫酸循環的過程中,下列說法正確的是____________(填字母序號)。
A. CO2光解變為CO和原子氧的變化為化學變化
B. SO3與水反應變為H2SO4為化合反應
C. CO變為CO2的過程中原子氧是催化劑
(5)金星被稱為“瘋狂”星球的原因是____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com