
【題目】通過化學學習,我們認識了“酸”和“堿”,請回答下列問題:
(1)常見的酸有硫酸、鹽酸等,在它們的水溶液里由于存在相同的(填符號),因此,它們有很多相似的化學性質,如:、 等(寫兩條即可).
(2)堿有氫氧化鈉、氫氧化鈣等,氫氧化鈉可作某些氣體的干燥劑,但不能干燥二氧化碳理由是 , 氫氧化鈣可由生石灰與水反應制得,反應的化學方程式為
(3)酸和堿能發生中和反應,它在日常生活和工農業生產中有廣泛的應用,如硫酸廠的污水中含有硫酸等雜質,可用熟石灰進行處理,反應的化學方程式為 .
(4)2010年4月14日青海玉樹大地震災害發生后,為了災區人民群眾的飲用水安全,衛生防疫部門要經常對災區水源進行監測,獲得可靠的科學依據.若現有一瓶水樣,要獲取它的酸堿度,應如何操作: .
(5)某化學興趣小組經過一段時間的調查與探究,模擬工廠的治污原理,設計了如圖所示裝置,一方排出含硫酸的廢水,另一方排出含氫氧化鈉的廢水,然后在池中混合,經充分反應后排放.若該工廠一天排出含氫氧化鈉10%的廢液400噸,需含硫酸9.8%的廢水多少噸才能完全中和? 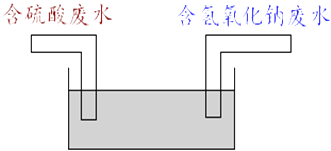
【答案】
(1)H+;能使紫色石蕊試液變紅,使無色酚酞試液不變色;能與堿發生中和反應
(2)氫氧化鈉能與二氧化碳反應;CaO+H2O=Ca(OH)2
(3)H2SO4+Ca(OH)2=CaSO4↓+2H2O
(4)取下一條pH試紙,用玻璃棒或膠頭滴管取少量待測液,滴在試紙上,等一會與標準比色卡對比,然后讀出pH的值
(5)解:設需含硫酸9.8%的廢水的質量為x
H2SO4+ | 2NaOH═Na2SO4+2H2O |
98 | 80 |
x98% | 400t×10% |
![]()
x=50t
答:需含硫酸9.8%的廢水的質量為50t
【解析】解:(1)①因為酸是在水溶液中電離出的陽離子全部是氫離子的化合物,所以酸在水溶液中具有相同的H+ , 故填H+;②回憶酸的通性可知:能使紫色石蕊試液變紅,使無色酚酞試液不變色;能與堿發生中和反應;能與較活潑金屬反應;能和金屬氧化物反應;能和部分鹽反應等;(2)氫氧化鈉等屬于堿,不能用來干燥酸性的氣體如二氧化碳和二氧化硫等,因為堿能與之反應;氫氧化鈣可由生石灰與水反應制得,反應的化學方程式為:CaO+H2O=Ca(OH)2; 故填:氫氧化鈉能與二氧化碳反應;CaO+H2O=Ca(OH)2;(3)熟石灰成分(Ca(OH)2)屬于堿,H2SO4是酸,酸堿中和反應生成鹽(CaSO4)和水(H2O),正確寫出反應物、生成物的化學式,再將方程式配平即可.
故反應方程式為:H2SO4+Ca(OH)2=CaSO4↓+2H2O;(4)取下一條pH試紙,用玻璃棒或膠頭滴管取少量待測液,滴在試紙上,等一會與標準比色卡對比,然后讀出pH的值;
故填:取下一條pH試紙,用玻璃棒或膠頭滴管取少量待測液,滴在試紙上,等一會與標準比色卡對比,然后讀出pH的值;
【考點精析】本題主要考查了中和反應及其應用和書寫化學方程式、文字表達式、電離方程式的相關知識點,需要掌握中和反應:酸與堿作用生成鹽和水的反應;注意:a、配平 b、條件 c、箭號才能正確解答此題.


科目:初中化學 來源: 題型:
【題目】推斷題:如圖所示,A、B物質是含有兩種相同元素的液體,G是黑色粉末的氧化物,E為生活中常見的銀白色金屬.圖中部分反應物和生成物均已省略.依題意回答下列問題: 
(1)物質G的名稱是 , 物質F的物質類別是 .
(2)E→D反應的化學方程式為 . 基本反應類型是 .
(3)E→F的反應中觀察到的實驗現象是化學方程式為.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】把某種金屬用小刀輕輕切下一小塊放入盛水的燒杯中,觀察到該金屬能與水劇烈反應,并放出熱,本身熔化成銀白色的小圓球,浮在水面上,根據以上敘述,推斷該金屬的物理性質有:①硬度;②熔點;③密度;④顏色 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某班學生以施用化肥的利與弊為題進行小組辯論,正方的觀點是施肥有利,正方的下列觀點中,不科學的是 ( )
A.施用化肥可以使農作物增加產量
B.化肥肥效快
C.施用化肥不會造成環境污染
D.復合肥能為農作物提供幾種營養素
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列有關金屬的說法正確的是( )
A.銅的導電性是金屬中最好的,故用于制作電線
B.鋁比鐵金屬活動性強,但鋁制品比鐵制品耐腐蝕
C.銅、黃銅、錫、焊錫都屬于單質
D.鍍鋅的“白鐵皮”不易生銹,說明鋅沒有鐵活潑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com