
【題目】現有一固體混合物A的成分,已知其中可能含有NH4C1、Na2SO4、CuCl2、NaCl、AgCl幾種物質中的兩種或多種。按下圖所示進行實驗,出現的現象如下圖中所述(設過程中所有可能發生的反應均恰好完全反應)。

試根據實驗過程和發生的現象填寫以下空白(均填寫相應的化學符號):
(1)混合物A中,一定不存在的物質是_________,可能存在的物質是_________。
(2)氣體B是_________,現象X為_________。
(3)濾液C中,存在的金屬陽離子是_________。
(4)濾渣D是_________。
(5)寫出實驗過程③中發生的化學反應的化學方程式________。
【答案】 AgCl NaCl NH3 酚酞試液變紅色 Na+ Cu(OH)2 BaCl2+Na2SO4=BaSO4↓+2NaCl
【解析】此題屬于敘述實驗型框圖推斷題,解題時,要緊跟實驗步驟,抓住特征現象,比如:特征顏色、特征離子的檢驗等。在固體A中加入NaOH溶液,產生一種氣體,將氣體通入酚酞溶液中,有現象,結合白色固體中的物質成分,可判斷含有NH4C1,氣體B為氨氣,在濾液C中加入BaCl2溶液,產生白色沉淀,可以判斷原白色固體中一定含有Na2SO4,在濾渣D中加入稀硫酸,得到藍色溶液,說明原白色固體中含有CuCl2。
解:(1)因為AgCl沉淀,且不溶于稀硫酸,所以混合物A中,一定不存在的物質是AgCl,可能存在的物質是:NaCl;
(2)經上面的分析,氣體B是NH3,氨氣溶于水形成氨水,呈堿性,所以現象X是:酚酞試液變紅色;
(3)濾液C中,存在的金屬陽離子是Na+;
(4)濾渣D是CuCl2與NaOH相互反應的生成物,是Cu(OH)2;
(5)實驗過程③中發生的化學反應的化學方程式是;BaCl2+Na2SO4=BaSO4↓+2NaCl。


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:
【題目】下列圖象不能正確反映實驗事實的是( )

A.向氫氧化鈉溶液中滴加過量的稀鹽酸
B.相同質量的鋅粉和鎂粉與等質量相同溶質質量分數的稀鹽酸(足量)反應
C.加熱氯酸鉀和二氧化錳的混合物
D.向硫酸銅溶液中滴加氫氧化鈉溶液
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某氣體既能用排水法收集,又能用向上排空氣法收集,該氣體具有的物理性質是( )
A.難溶于水,密度比空氣大 B.難溶于水,密度比空氣小
C.易溶于水,密度比空氣大 D.易溶于水,密度比空氣小
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列事實中符合質量守恒定律的是( )
①蠟燭燃燒后,其質量變小;②鐵絲燃燒后,生成物質量比鐵絲的大了
③濕衣服晾干后,質量變小;④高錳酸鉀受熱分解后,剩余固體質量比原固體的減少
A.①②③ B.①②④ C.①②③④ D.只有③
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】小明按照課本實驗(如圖1)探究分子的運動時,聞到了刺激性的氨味.在老師的指導下,小明設計了如圖2的實驗裝置,進行同樣的實驗,結果不再聞到刺激性的氨味,并立即觀察到明顯的實驗現象,得到了和課本實驗同樣的結論.

【實驗與結論】請你幫助小明完成圖2裝置的實驗,回答下列問題.
(1)滴入少量濃氨水后,濕潤的滴有酚酞溶液的濾紙條變成紅色.從微觀的角度分析,此現象說明_____________________________;從濃氨水化學性質的角度分析,此現象說明濃氨水呈________________.
(2)固體氫氧化鈉的作用是__________________________________.
(3)與課本實驗比較,小明改進后的裝置的優點是(寫出一點)______________________.
【繼續探究】小英受小明實驗的啟發,將圖2裝置進一步改裝成圖3裝置,用于驗證二氧化碳的性質.
(4)打開活塞K滴入稀硫酸,兩條用紫色石蕊溶液潤濕的濾紙現象差別是________ 先變紅。小英從課本實驗中知道,二氧化碳和水本身都不能使石蕊溶液變色,因而她認為以上的現象差別驗證的二氧化碳性質是____________________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某校化學小組在利用硫酸和氫氧化鈉溶液探究酸堿中和反應時,利用數字化傳感器測得燒杯中溶液pH的變化,其圖象如圖所示,下列說法正確的是
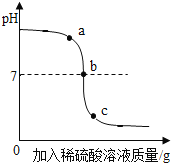
A.圖中c點所示溶液呈堿性
B.圖中a點所示溶液中,含有的溶質是Na2SO4和H2SO4
C.該實驗是將氫氧化鈉溶液逐滴滴入到盛有硫酸的燒杯中
D.由a點到b點的pH變化過程證明酸和堿發生了中和反應
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】黃鐵礦(主要成分為FeS2,雜質不含硫元素)是我國大多數硫酸廠制取硫酸的主要原料。化學課外活動小組為測定某黃鐵礦中FeS2含量進行了如下的實驗探究(假設每步反應均完全)。
【查閱資料】 ①4FeS2+11O2 ![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
②Na2SO3+H2O2=Na2SO4+H2O
【實驗探究】
Ⅰ. 稱取2.40 g黃鐵礦樣品放入下圖所示裝置(夾持和加熱裝置省略)的石英管中,從a處不斷地緩緩通入空氣,高溫灼燒石英管中的黃鐵礦樣品至反應完全。
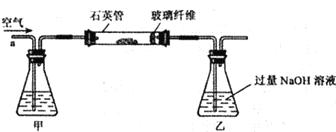
Ⅱ. 反應結束后,將乙瓶中的溶液進行如下處理:
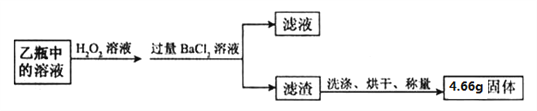
【問題討論】
(1)Ⅰ裝置中甲瓶內盛放的試劑是氫氧化鈉溶液,其作用是______________。
(2)Ⅰ裝置中乙瓶內發生反應的化學反應方程式是____________________。
【含量測定】
(3)計算該黃鐵礦中FeS2的質量分數__________________。(請寫出計算過程)
【交流反思】
(4)如果缺少甲裝置,則最終測得FeS2的質量分數將會________________(填“偏大”“偏小”或“不變”)。
(5)Ⅱ中檢驗濾渣是否洗滌干凈的方法是,取最后一次洗滌液,加入_____________,說明已洗滌干凈。
【拓展應用】
工業上以黃鐵礦為原料生產硫酸的工藝流程圖如下所示:
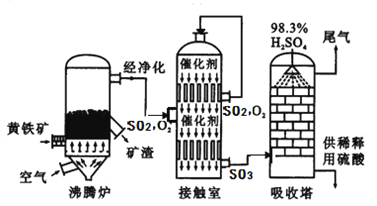
(6)接觸室中發生反應的化學方程式為________________________。化學實驗室常需要用到較稀的硫酸,把濃硫酸稀釋的操作是_______________________________________,硫酸是一種重要的化工產品,用途十分廣泛,請寫出稀硫酸的一種用途______________________。
(7)依據生產硫酸的工藝流程圖,下列說法正確的是_______________(填字母)。
A.為使黃鐵礦充分燃燒,需將其粉碎 B.催化劑能夠提高SO2的反應速率和產量
C.沸騰爐排出的礦渣可供煉鐵 D.吸收塔中為了提高吸收效率,采用噴淋的方式
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com