
【題目】通過海水提取的粗鹽中含有 MgCl2、CaCl2、MgSO4.以及泥沙等雜質.以下是一種 制備精鹽的實驗方案(用于沉淀的試劑均過量).
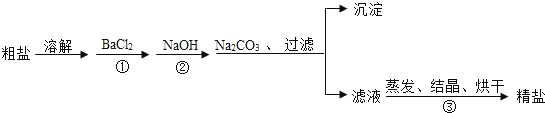
請回答下列問題:
(1)寫出②中反應的化學方程式___________________________.
(2)加入 BaCl2、NaOH、Na2CO3 的順序還可以改變嗎?若能改變則寫出改變的順序,若不能改變,請說明理由_______________________________________.
(3)該實驗方案還需完善,請寫出具體的操作步驟___________________________________________.
【答案】2NaOH+MgCl2=Mg(OH)2↓+2NaCl BaCl2、Na2CO3、NaOH 向濾液中加入適量的稀鹽酸
【解析】
(1)②中的反應是氫氧化鈉和氯化鎂反應生成氫氧化鎂沉淀和氯化鈉,化學方程式為:2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
(2)氯化鋇與硫酸鎂反應生成硫酸鋇和氯化鎂,氯化鋇的作用是除去硫酸鎂;氫氧化鈉和氯化鎂反應生成氫氧化鎂沉淀和氯化鈉,氫氧化鈉的作用是除去氯化鎂;碳酸鈉與氯化鋇、氯化鈣反應分別生成碳酸鋇、碳酸鈣和氯化鈉,碳酸鈉的作用是除去過量的氯化鋇和氯化鈣,碳酸鈉必須放在氯化鋇之后,與氫氧化鈉的順序部分先后,所以改變的順序是:BaCl2、Na2CO3、NaOH;
(3)過濾后濾液的主要成分有:NaCl、NaOH、Na2CO3;要得到純凈的氯化鈉,此實驗方案尚需完善,具體步驟是:向濾液中加入適量的稀鹽酸,以除去氫氧化鈉和碳酸鈉。
。


 高效智能課時作業系列答案
高效智能課時作業系列答案 捷徑訓練檢測卷系列答案
捷徑訓練檢測卷系列答案 小夫子全能檢測系列答案
小夫子全能檢測系列答案科目:初中化學 來源: 題型:
【題目】下表是三種物質在不同溫度時的溶解度,根據表中信息回答問題。
溫度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 氯化鈉 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
硝酸鉀 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
氫氧化鈣 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
(1)60℃時,氯化鈉的溶解度_______硝酸鉀的溶解度(填“>”“=”或“<”)。
(2)20℃時,氯化鈉飽和溶液中溶質的質量分數為_______(結果保留至0.1%)。
(3)如圖所示,觀察到U型管中a的液面低于b的液面,澄清石灰水_____________,則在小試管中加入的物質是_____(填字母)。
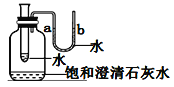
A.濃硫酸 B.氫氧化鈉 C.硝酸銨
(4)混有少量氯化鈉的硝酸鉀固體,加水配成80℃的硝酸鉀飽和溶液,再冷卻至20℃,析出晶體并得到溶液。下列有關說法中正確的是_______(填字母)。
A.析出的晶體中不一定含有硝酸鉀
B.所得溶液一定是硝酸鉀飽和溶液
C.上述方法可以將兩種物質完全分離
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】酸、堿、鹽在生產和生活中有著廣泛的應用。
(1)氫氧化鈉溶液和氫氧化鈣溶液都能使酚酞溶液變紅,其原因是二者的溶液中均含有相同的粒子________(填粒子符號)。
(2)鈉與水反應,生成一種堿和密度最小的氣體,該反應的化學方程式為___________。
(3)向一定量的稀鹽酸和氯化鎂的混合溶液中,逐滴加入10%的氫氧化鈉溶液至過量,并測得溶液的pH隨加入氫氧化鈉溶液質量的變化曲線如圖所示。
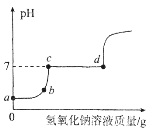
①b點溶液中含有哪些溶質__________________?(寫化學式)
②寫出c→d段反應的化學方程式__________________。
(4)某同學為了除去食鹽水中的MgCl2、CaCl2、Na2SO4等雜質,設計了如圖所示的實驗方案。
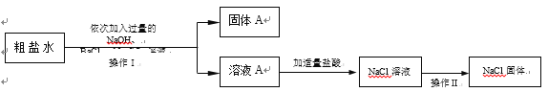
①操作II中玻璃棒的作用是___________?
②加入過量Na2CO3溶液的作用是____________________。
③寫出該實驗過程中發生的中和反應的化學方程式__________。
(5)為測定某石灰石樣品中碳酸鈣的質量分數,稱取10 g石灰石(雜質不參加反應)放入燒杯中,加入100 g稀鹽酸,二者恰好完全反應,反應后燒杯中剩余物質的總質量為106.7 g(氣體的溶解忽略不計)。請計算該樣品中碳酸鈣的質量分數__________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】將爐甘石(ZnCO3)、赤銅(Cu2O)和木炭粉(C)混合后加熱到約800℃,得到一種鋅和銅的合金——黃銅,外觀似黃金但質地堅硬。
(1)上述物質中,屬于氧化物的是_________。
(2)赤銅(Cu2O)中銅的化合價為______,800℃時,赤銅和木炭粉發生置換反應生成的單質是_________。
(3)已知![]() ,若原料中含25噸ZnCO3 ,請列式計算充分反應后,理論上所得黃銅中鋅的質量_________。
,若原料中含25噸ZnCO3 ,請列式計算充分反應后,理論上所得黃銅中鋅的質量_________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(1)圖1裝置中既能制O2又能制CO2的是_____(填序號)。
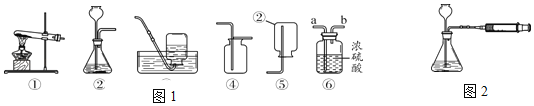
請寫出實驗室用你所選裝置制兩種氣體的化學方程式。
制O2:_____。
制CO2:_____。
(2)用推拉注射器活塞的方法來檢查裝置氣密性,如圖2,當緩慢拉動活塞時,如果裝置氣密性良好,則能觀察到_____。
(3)實驗室常用澄清石灰水檢驗CO2,寫出反應的化學方程式:_____。
(4)某些大理石中含少量硫化物,使制得的CO2中混有H2S氣體。欲獲取純凈、干燥的CO2,需對發生裝置中產生的氣體進行除雜,實驗裝置如圖3所示:
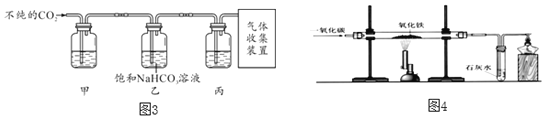
查閱資料:
Ⅰ.H2S能與NaOH等堿溶液、CuSO4溶液反應;
Ⅱ.CO2中混有的HCl氣體可用飽和NaHCO3溶液吸收。
①裝置甲中所盛試劑應選用_____(填字母序號)。
A.濃硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO4溶液
②裝置丙的作用是_____。
(5)煉鐵的原理是利用一氧化碳與氧化鐵反應。在實驗室里,可用圖4所示裝置進行實驗:實驗中玻璃管內的粉末由紅色變為_____色,該反應的化學方程式為_____,通過實驗我可以得出的一氧化碳的相關化學性質是_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖中A、B、C、D是四種粒子的結構示意圖。
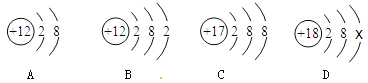
請回答下列問題:
(1)圖中A、B、C、D屬于_______種元素的粒子;
(2)A、B、C、D四種粒子中,不具備穩定結構的是_________(填序號);
(3)D中x=________;
(4)A與C形成化合物的化學式是___________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為了探究金屬與酸反應的規律,某實驗小組進行了如下實驗,取等質量的鐵片、鎂片、鋅片,分別與等體積、等濃度的稀鹽酸反應,用溫度傳感器測得反應溫度變化曲線如下圖所示。
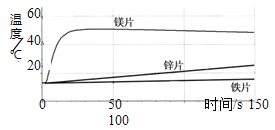
(1)請分析反應中溫度升高的原因:_________________ ;
(2)根據曲線總結出金屬活動性的相關規律:__________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】氧是地殼中含量最多的元素,氧及其化合物是化學學習和研究的重要內容。
(1)從下圖的原子結構示意圖中獲得的信息,正確的是_______________(填標號)。
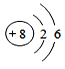
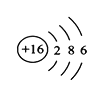
a ![]() 表示原子核,帶8個單位正電荷
表示原子核,帶8個單位正電荷
b 氧原子核外有2個電子層,有8個電子在核外作高速運動
c 氧原子在化學反應中易失去電子形成離子(O2-)
d 這兩種原子屬于同一種元素,化學性質相似
(2)從微觀角度:用“![]() ”表示氧原子。用“
”表示氧原子。用“![]() ”可表示的微粒是_________(填名稱,下同),構成氧分子的微粒是______,氧氣經降溫和加壓變為液態氧后體積變小,用微粒的觀點解釋之:____________。
”可表示的微粒是_________(填名稱,下同),構成氧分子的微粒是______,氧氣經降溫和加壓變為液態氧后體積變小,用微粒的觀點解釋之:____________。
(3)自然界中氧循環的環節之一:綠色植物的光合作用,有關反應的化學方程式6CO2+6H2O C6H12O6+XO2 ,則X=________,綠色植物通過光合作用將太陽能轉化為______能。
C6H12O6+XO2 ,則X=________,綠色植物通過光合作用將太陽能轉化為______能。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】由于溶解度不同(如圖所示),飽和碳酸鈉溶液中通入CO 2會析出碳酸氫鈉晶體而使溶液變渾濁。某化學課外小組同學發現不同條件下出現渾濁的時間不同。
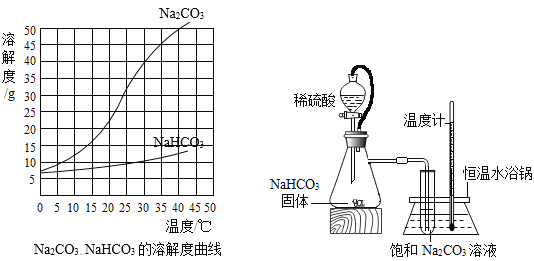
(提出問題)影響碳酸氫鈉晶體產生速率的因素有哪些?
(猜想與假設)碳酸氫鈉晶體產生速率的影響因素有溫度、試管內徑、CO2流速、飽和碳酸鈉溶液的體積。
(進行實驗)實驗裝置如圖所示。每次實驗時均在試管里加入1mL飽和碳酸鈉溶液并在試管后放置一張寫有黑色字跡的白紙,從垂直于試管的方向觀察白紙上字跡的清晰程度,記錄時間,用于判斷碳酸氫鈉晶體的產生速率。部分實驗記錄如下表所示:
序號 | 溫度(℃) | 試管內經(mm) | CO2流速 (個氣泡/s) | 產生不同現象的時間(s) | ||
字跡變淺 | 字跡模糊 | 字跡消失 | ||||
① | 25 | 10 | 5~8 | 517" | 719" | 817" |
② | 32 | 10 | 5~8 | 350" | 409" | 428" |
③ | 40 | 10 | 5~8 | 348" | 406" | 418" |
④ | 25 | 14 | 5~8 | 636" | 738" | 828" |
⑤ | 25 | 25 | 5~8 | X | 943" | 1022" |
⑥ | 25 | 10 | 10~13 | 502" | 640" | 758" |
⑦ | 25 | 10 | 2~5 | 540" | 1045" | 1236" |
(解釋與結論)
(1)由上述溶解度曲線圖可知溶解度受溫度影響相對更大的物質是_________________。
(2)錐形瓶中是利用碳酸氫鈉與稀硫酸反應來制取二氧化碳。除生成二氧化碳外,還有水和硫酸鈉生成,該反應的化學方程式為_____________________。
(3) 同學們若要研究飽和碳酸鈉溶液的體積對碳酸氫鈉晶體產生速率是否有影響,需要控制的變量有__________________。
(4)由實驗①②③,可得出的結論是____________________。
(5)實驗①④⑤研究的影響因素是___________________。
(6)通過對數據的觀察和分析,小倩認為“二氧化碳流速越快,碳酸氫鈉晶體產生速率越快”,得到該結論的依據是______________(填實驗序號)。
(反思與評價)
(7)表中X的取值范圍應該是_______________。
(8)該實驗采用硫酸而不是鹽酸來制備二氧化碳的原因是__________________。
(9)如圖中使用橡皮管連接分液漏斗與錐形瓶的目的是__________________。
(10)如何除去碳酸鈉中混有的少量碳酸氫鈉?___________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com