
【題目】二百多年前,法國化學家拉瓦錫用定量的方法研究了空氣的成分。仿照這個歷史上著名實驗的原理,我們可以用圖1所示裝置來測定空氣中氧氣的含量。

【提出問題】用紅磷燃燒的方法為什么測出的氧氣含量遠低于21%?
【分析討論】(1)實驗裝置漏氣;(2)________________,導致裝置內氧氣有剩余;(3)……
【實驗與交流】在老師的指導下,同學們查閱了白磷、紅磷等物質燃燒需要的最低含氧量如下:
資料1:
可燃物名稱 | 紅磷 | 白磷 | 蠟燭 |
最低含氧量/% | 8.0 | 4.0 | 16.0 |
甲、乙、丙三個小組分別用上述過量紅磷、白磷、蠟燭三種物質進行該實驗,用測氧氣濃度的傳感器測得反應后的氧氣濃度分別為8.85%、3.21%、16.7%,數據與表中的理論值基本一致。其中蠟燭燃燒后用測一氧化碳濃度傳感器測算一氧化碳濃度約為2%。
資料2:蠟燭或者木炭在密閉的集氣瓶中燃燒,氧氣濃度會不斷變小,會有一氧化碳氣體生成。常溫下一氧化碳難溶于水,且不與澄清石灰水反應。根據以上信息回答下列問題:
(1)白磷和紅磷相比,使用白磷能使結果更準確,其原因是_______________________。
(2)請寫出紅磷燃燒的化學方程式______________,該反應屬于___________反應(填一種基本反應類型);有同學提議選用木炭替代紅磷做實驗,在集氣瓶底部預先放少量澄清石灰水吸收生成的二氧化碳氣體,小華覺得不可行,其主要原因是________________。
(3)興趣小組用白磷代替紅磷進行實驗,已知化學反應前后元素種類和質量都不發生改變,若該實驗中消耗的氧氣質量為0.8克,則理論上生成的五氧化二磷的質量為______。
【實驗拓展】某校研究性學習小組用下圖裝置進行鎂條在空氣中燃燒的實驗。燃燒、冷卻后打開止水夾,進入集氣瓶中水的體積約占集氣瓶體積的70%。
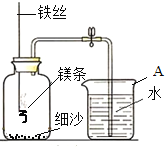
(4)實驗過程中,若彈簧夾未夾緊,則進入集氣瓶中的水會_______(選填“偏大”、“偏小”或“不變”)。
(5)如果鎂條只和空氣中的氧氣反應,則進入集氣瓶中水的體積最多不超過其容積的_______,現進入集氣瓶中水的體積約為其容積的 70%,根據空氣的組成可推出減少的氣體中還一定有氮氣,其理由是______________________。
【提出問題】氮氣是怎樣減少的呢?
【作出假設】氮氣是與鎂條反應而減少的。
【查閱資料】
①鎂條在空氣中燃燒時,不僅與空氣中的氧氣反應生成氧化鎂,還能與氮氣反應生成氮化鎂(氮化鎂中氮元素的化合價為-3價),請寫出鎂條與氮氣反應的化學方程式__________;
②鎂條除了能與氮氣反應,還可以在二氧化碳氣體中燃燒生成碳和氧化鎂,請你寫出該反應的化學方程式___________
【驗證實驗】用坩堝鉗夾持鎂條,點燃后迅速伸入盛有氮氣的集氣瓶中,鎂條燃燒,發出暗紅色火焰,生成淡黃色粉末,并放出大量的熱。
【得出結論】鎂條能在氮氣中燃燒生成固體氮化鎂。
【實驗反思】通過以上實驗探究,我們可以知道用于測定空氣中氧氣含量所選用的藥品,應符合的條件是____________________。
【答案】 紅磷的量不足 白磷消耗氧氣更充分 4P+5O2![]() 2P2O5 化合 木炭在氧氣濃度較低時,會生成CO氣體,且CO氣體難溶于水,不與澄清石灰水反應 1.42 偏大 21%或1/5 氮氣約占空氣組成的78%,大于49% 【答題空10】3Mg+N2
2P2O5 化合 木炭在氧氣濃度較低時,會生成CO氣體,且CO氣體難溶于水,不與澄清石灰水反應 1.42 偏大 21%或1/5 氮氣約占空氣組成的78%,大于49% 【答題空10】3Mg+N2![]() Mg3N2 2Mg+CO2
Mg3N2 2Mg+CO2![]() 2MgO+C 只與空氣中的氧氣發生反應
2MgO+C 只與空氣中的氧氣發生反應
【解析】【提出問題】用紅磷燃燒的方法為什么測出的氧氣含量遠低于21%?【分析討論】(1)實驗裝置漏氣;(2)紅磷的量不足,導致裝置內氧氣有剩余;【實驗與交流】資料1:資料2:(1)白磷和紅磷相比,使用白磷能使結果更準確,其原因是白磷消耗氧氣更充分。(2)紅磷燃燒的化學方程式∶4P+5O2 ![]() 2P2O5,該反應屬于化合反應,兩種物質生成了一種物質;用木炭替代紅磷做實驗,在集氣瓶底部預先放少量澄清石灰水吸收生成的二氧化碳氣體,小華覺得不可行,其主要原因是木炭在氧氣濃度較低時,會生成CO氣體,且CO氣體難溶于水,不與澄清石灰水反應。(3)用白磷代替紅磷進行實驗,若該實驗中消耗的氧氣質量為0.8克,則理論上生成的五氧化二磷的質量為∶
2P2O5,該反應屬于化合反應,兩種物質生成了一種物質;用木炭替代紅磷做實驗,在集氣瓶底部預先放少量澄清石灰水吸收生成的二氧化碳氣體,小華覺得不可行,其主要原因是木炭在氧氣濃度較低時,會生成CO氣體,且CO氣體難溶于水,不與澄清石灰水反應。(3)用白磷代替紅磷進行實驗,若該實驗中消耗的氧氣質量為0.8克,則理論上生成的五氧化二磷的質量為∶
4P+5O2 ![]() 2P2O5
2P2O5
160 284
0.8g x
![]() =
=![]() ,x=1.42g.
,x=1.42g.
【實驗拓展】鎂條在空氣中燃燒的實驗。(4)實驗過程中,若彈簧夾未夾緊,則進入集氣瓶中的水會偏大。(5)如果鎂條只和空氣中的氧氣反應,則進入集氣瓶中水的體積最多不超過其容積的21%或1/5,現進入集氣瓶中水的體積約為其容積的 70%,根據空氣的組成可推出減少的氣體中還一定有氮氣,其理由是氮氣約占空氣組成的78%,大于49%。【提出問題】氮氣是怎樣減少的呢?【作出假設】氮氣是與鎂條反應而減少的。【查閱資料】
①鎂條在空氣中燃燒時,不僅與空氣中的氧氣反應生成氧化鎂,還能與氮氣反應生成氮化鎂(氮化鎂中氮元素的化合價為-3價),鎂條與氮氣反應的化學方程式3Mg+N2 ![]() Mg3N2 ,根據正負總價代數和為零原則,氮化鎂化學式是Mg3N2;
Mg3N2 ,根據正負總價代數和為零原則,氮化鎂化學式是Mg3N2;
②鎂條除了能與氮氣反應,還可以在二氧化碳氣體中燃燒生成碳和氧化鎂,該反應的化學方程式∶2Mg+CO2 ![]() 2MgO+C。【驗證實驗】用坩堝鉗夾持鎂條,點燃后迅速伸入盛有氮氣的集氣瓶中,鎂條燃燒,發出暗紅色火焰,生成淡黃色粉末,并放出大量的熱。【得出結論】鎂條能在氮氣中燃燒生成固體氮化鎂。【實驗反思】用于測定空氣中氧氣含量所選用的藥品,應符合的條件是只與空氣中的氧氣發生反應,生成物只能是固體。
2MgO+C。【驗證實驗】用坩堝鉗夾持鎂條,點燃后迅速伸入盛有氮氣的集氣瓶中,鎂條燃燒,發出暗紅色火焰,生成淡黃色粉末,并放出大量的熱。【得出結論】鎂條能在氮氣中燃燒生成固體氮化鎂。【實驗反思】用于測定空氣中氧氣含量所選用的藥品,應符合的條件是只與空氣中的氧氣發生反應,生成物只能是固體。
點睛∶這是一道實驗探究題,主要探究通過實驗測定空氣中氧氣的含量,本實驗成功的關鍵①裝置氣密性良好②反應物過量,生成物只能是固體③冷卻后測量。


 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:初中化學 來源: 題型:
【題目】某實驗小組在實驗室里制取二氧化碳時,用到了如圖所示裝置,請回答有關問題:
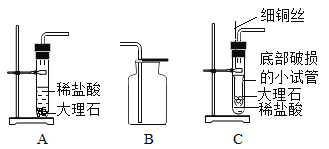
(1)能用B裝置收集二氧化碳,是因為二氧化碳的密度比空氣____。
(2)用B裝置收集二氧化碳時,檢驗是否收集滿的方法是將____的木條放在____。
(3)二氧化碳常用于滅火。是因為二氧化碳具有____的性質。
(4)將生成的二氧化碳通入石蕊試液中,試液變紅,原因是反應生成的____使石蕊變色的。寫出此反應的文字表達式____。
(5)將A裝置改成C裝置,通過拉動銅絲可以控制底部破損的小試管升降。這改進的 主要目的是____(填字母序號)
A.使反應隨時發生或停止B.使破損的小試管得到利用C.生成更多的二氧化碳
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】維生素C(化學為C6H8O6)主要存在于蔬菜、水果中,它能促進人體生長發育,增強人體對疾病的抵抗力。下列關于維生素C的說法錯誤的是 ( )
A. 維生素C的相對分子質量是176
B. 維生素C中碳元素的質量分數為40.9%
C. 維生素C是由碳元素、氧元素和氫元素組成
D. 維生素C中C、H、O三種元素的質量比為6∶8 ∶6
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在化學實驗中,從試劑瓶中取出的藥品使用后有剩余,正確的處置方法是( )
A. 帶出實驗室 B. 放回原試劑瓶
C. 在實驗室集中處理 D. 投入通向下水道的水槽內
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】現有符號①2O ②N2 ③2O3 ④2CO ⑤2N3- ⑥SO42- ⑦3Fe3+ ⑧H2O ⑨![]() ,其中數字“2”表示的含義不同,下列判斷正確的是( )
,其中數字“2”表示的含義不同,下列判斷正確的是( )
A. 表示分子個數:①③ B. 表示離子個數:⑤⑦
C. 表示原子個數:②④⑧ D. 表示化合價:⑥⑨
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(1)在①膽礬(CuSO4·5H2O) ②稀有氣體 ③氯酸鉀 ④四氧化三鐵 ⑤蒸餾水 ⑥空氣 ⑦鋅 ⑧澄清石灰水 ⑨液氧和氧氣混合物中,屬于混合物的是_______________;屬于化合物的是_______________;
(2)下圖是表示氣體分子的示意圖,圖中“●”和“”分別表示兩種不同質子數的原子,其中可能表示氧化物的是_______________(填序號)。
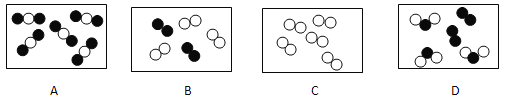
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖是第三周期部分元素的微粒結構示意圖,請根據題目要求填空。
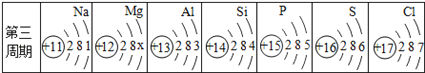
(1)上圖中x=____________。
(2)硫原子的質子數為____________,鋁原子的最外層電子數為____________。
(3)某粒子的結構示意圖為![]() ,當a-b=8時,該粒子的符號為____________。
,當a-b=8時,該粒子的符號為____________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】太陽能吸附式制冷結露法空氣取水器可用于野外獲取淡水,工作原理如下圖所示。
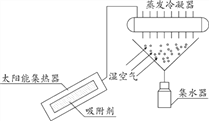
(1)蒸發冷凝器中發生的是_______(填“物理”“化學”)變化。
(2)吸附劑中主要物質為SiO2和CaCl2,SiO2中硅元素的化合價為________,CaCl2中鈣、氯元素的質量比為________。
(3)如下圖所示,電子秤上的量筒中盛有蒸餾水,放置一段時間,電子秤示數變小,從微粒的角度解釋其原因是______。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com