
【題目】分析化學反應:2H2S+3O2![]() 2SO2+2H2O,化學反應前后化合價有改變的元素是( )
2SO2+2H2O,化學反應前后化合價有改變的元素是( )
A.硫和氧B.氫和氧C.只有硫D.氫、硫、氧
 出彩同步大試卷系列答案
出彩同步大試卷系列答案科目:初中化學 來源: 題型:
【題目】將等質量的甲乙兩種固體分別加入到等質量 t0℃的水中充分溶解后均有固體剩余,升高溫度到 t3℃剩余固體質量隨溫度的變化情況如圖下列說法錯誤的是( )
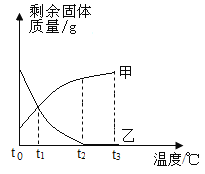
A.t2℃時,甲乙兩種物質的溶解度甲 >乙
B.t3℃時,甲是飽和溶液
C.t0℃ ~t2℃乙物質的溶解度隨溫度升高而增大
D.將溫度從 t2℃降至 t1℃時,甲乙兩溶液的溶質質量分數相等
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖表示的是甲、乙兩種物質的溶解度曲線,據圖所示,下列說法正確的是( )
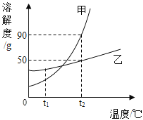
A. t2℃時,甲乙兩物質飽和溶液中的溶質質量大小關系是甲>乙
B. 若甲物質中混有少量的乙物質,可以采用降溫結晶的方法提純甲物質
C. t2℃時將30g乙物質加入到50g水中,所得溶液的質量為80g
D. 將t1℃的甲、乙兩物質的飽和溶液(均無固體物質剩余)升溫到t2℃時,溶液中的溶質質量分數大小關系是甲>乙
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列實驗能達到實驗目的的是( )
A. 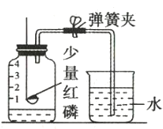 探究空氣中氧氣含量
探究空氣中氧氣含量
B. 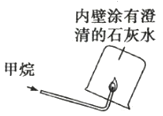 驗證甲烷(CH.4)燃燒生成二氧化碳和水
驗證甲烷(CH.4)燃燒生成二氧化碳和水
C.  探究反應物濃度對反應速率的影響
探究反應物濃度對反應速率的影響
D.  探究分子運動
探究分子運動
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】天然氣的主要成分是甲烷(CH4),實驗室將固體醋酸鈉(CH3COONa)與堿石灰(NaOH和CaO的混合物)共熱來制取甲烷氣體,反應的原理是:CH3COONa+NaOH![]() Na2CO3+CH4↑結合如圖回答下列問題:
Na2CO3+CH4↑結合如圖回答下列問題:
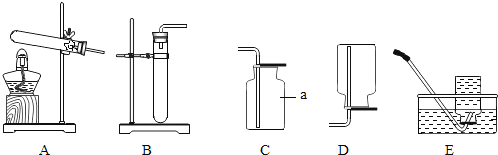
(1)儀器a的名稱是_____;制取甲烷的發生裝置是_____(填字母序號),理由是____.
(2)甲烷是無色、無味的氣體,可采用D或E的裝置來收集甲烷,請補充完整甲烷的物理性質___.
(3)甲烷像氫氣一樣是易燃氣體,點燃前應該進行的操作是___,寫出甲烷燃燒的化學方程式____.
(4)要產生32g甲烷氣體,至少需要醋酸鈉粉末的質量是____g
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】酸、堿、鹽參與的化學反應有一定的規律。
(1)取少量氫氧化鈉溶液于燒杯中,滴入幾滴酚酞試液,在攪拌下,再逐滴加入稀鹽酸至溶液變成無色,此時溶液的pH較之前_____(填“升高”“降低”或“不變”),若用實驗證明酚酞仍存在于溶液中,你的實驗操作方法是_____,現象是_____。
(2)已知反應:酸(稀)+X→CuSO4+水,若X為金屬氧化物,該反應的化學方程式是_____;若該反應為中和反應,則X物質是_____。
(3)CuSO4溶液不宜用鐵制容器盛裝,原因是_____(用化學方程式表示)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(1)自然界中吸收大氣中CO2的最重要環節是_____.
(2)科學家研究得到:海洋是吸收大量CO2的地方.如果CO2排放量繼續增加,海洋將被“酸化”.請寫出海洋酸化原因的化學方程式________.
(3)科學家目前正在研究將空氣中過量的CO2和H2在催化劑和適量條件下轉化成液態甲醇和水,反應的化學方程式:CO2+3H2 甲醇+H2O.則甲醇的化學式是______.
甲醇+H2O.則甲醇的化學式是______.
(4)已知20℃時,KCl的溶解度為34克,50℃時的溶解度為42.6克.通過以下實驗操作得到溶液①至⑤:
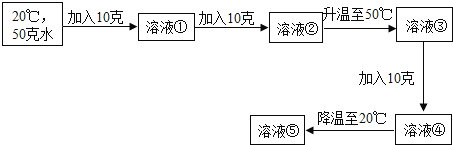
Ⅰ、上述實驗所得溶液中,屬于飽和溶液的是____;
Ⅱ、溶液④的質量為____克;
Ⅲ、溶液⑤中,溶質的質量分數為_____.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據質量守恒定律的有關內容回答下列問題:
①15 mL酒精與15 mL水混合后的體積___(填“大于”“小于”或“等于”)30 mL,這是因為 __________,該變化_______(填“能”或“不能”)用質量守恒定律解釋,理由是__________________________。
②將6 g碳在18 g氧氣中燃燒,完全反應后得到的二氧化碳質量_______________(填“大于”“小于”或“等于”)24 g,這是因為__________________________________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某研究性學習小組以“酸與堿能否發生反應”為課題進行了實驗探究。
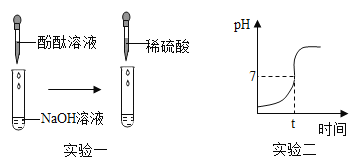
(實驗一)
(1)向滴有酚酞試液的NaOH溶液中滴入稀硫酸,觀察到溶液顏色由_____,證明硫酸和氫氧化鈉發生了反應,該反應的化學方程式為_____。
(2)繼續往上述反應后的溶液中逐滴滴入NaOH溶液,不斷振蕩,如果觀察到_____現象,證明了滴加的稀硫酸過量。
(實驗二)測量酸和堿反應過程的pH
(1)實驗過程中用傳感器實時獲得溶液的pH,要得到如圖所得變化曲線,所進行的操作是_____(填字母)。
A 將稀硫酸溶液逐滴滴加到氫氧化鈉溶液中
B 將氫氧化鈉溶液逐滴滴加到稀硫酸溶液中
(2)根據如圖2溶液pH變化,判斷酸和堿發生反應的依據是_____。
(實驗三)小組同學經過討論,一致認為除了上述方法外,還可以按照如表實驗方法證明硫酸和氫氧化鈉發生了反應。
實驗步驟 | 實驗現象 | 實驗結論 |
取少量氫氧化鈉溶液于試管中,加入過量的稀硫酸,再加入少量的氧化銅 | 得到藍色溶液,無_____ | 氫氧化鈉和硫酸發生了化 學反應 |
(拓展延伸)同學們對氫氧化鈉溶液和稀硫酸反應后溶液中的溶質成分產生了濃厚的興趣,于是進行了進一步的探究。
(提出問題)氫氧化鈉溶液和稀硫酸反應后溶液中的溶質成分
(提出猜想)猜想一:Na2SO4猜想二:Na2SO4和H2SO4你的合理猜想是:_____。
(進行實驗)
實驗步驟 | 實驗現象 | 實驗結論 |
取少量反應后的溶液置于試管中_____ | _____ | 猜想二正確 |
(實驗反思)在分析化學反應后所得物質成分時,除考慮生成物外還需要考慮反應物是否有剩余。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com