
【題目】醫用氯化鈣常用于合成藥物。以工業碳酸鈣(含少量Fe3+等雜質)為原料生產二水合氯化鈣(CaCl2·2H2O)的流程圖如下所示。
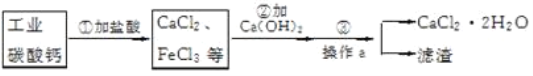
(1)寫出第①步中碳酸鈣與鹽酸反應的化學方程式:_____。
(2)第②步中是否發生化學變化?_____(填“是”或“否”)。
(3)操作a的名稱是_____,實驗室進行該操作時玻璃棒的作用是_____。
(4)青少年正處于生長發育階段,需要攝入足夠的鈣,寫出一種合理的補鈣方法:_____。
 新題型全程檢測期末沖刺100分系列答案
新題型全程檢測期末沖刺100分系列答案科目:初中化學 來源: 題型:
【題目】國際上有銦等七種元素的相對原子質量采用了我國科學家張青蓮測定的數據。下列有關銦的說法正確的是( )
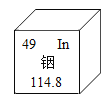
A. 核電荷數為 49
B. 相對原子質量為 114.8g
C. 屬于非金屬元素
D. 與其它元素的根本區別是中子數不同
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖“五連環”中的每一環表示一種物質,相連環物質間能發生反應,不相連環物質間不能發生反應。請完成下列問題:

(1)選擇氧氣、鐵、二氧化碳、氧化鈣、稀硫酸、燒堿溶液、氯化鋇溶液、碳酸鈣中的五種物質(所選物質至少包括“單質、氧化物、酸、堿、鹽”中的四種類型),將其化學式分別填入對應的環內_____。
(2)“五連環”中物質間發生的反應,沒有涉及的基本反應類型是_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】中和反應在日常生活中應用廣泛,下列是稀鹽酸和氫氧化鈉溶液反應的微觀示意圖。回答以下問題:
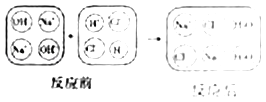
(1)分析圖中反應前后沒有發生變化的微粒是_____、_____;反應的實質是_____。
(2)如果規定上述反應后溶液的pH<7,顯酸性。請你設計一個實驗方案證明溶液顯酸性:
實驗操作 | 實驗現象 | 實驗結論 |
①______ | ②______ | 顯酸性 |
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某純堿樣品中含有少量NaCl,小麗同學取該樣品23g全部溶解于150g水中,再逐滴加入160g稀鹽酸,反應中產生的氣體的質量與鹽酸的用量關系如圖所示。(提示:相關反應為Na2CO3+2HCl=2NaCl+H2O+CO2↑)計算當恰好完全反應時:
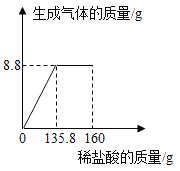
(1)產生的二氧化碳的質量是 克。
(2)此時所得到的溶液中溶質的質量分數(寫出必要的計算過程,結果保留到0.1%)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖是某化學興趣小組。設計的金屬活動性順序的探究實驗。
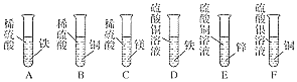
(1)上述實驗中,有氣泡生成的是________(填寫裝置序號)。
(2)試管F中出現的實驗現象是______________。
(3)上述實驗能否證明鎂、鋅、鐵、銅、銀五種金屬的活動性強弱?____請說明理由_____。
(4)我國古代“濕法煉銅”就是利用了試管D中的反應原理,請寫出該反應的化學方程式:______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下表是NaCl、KNO3在不同溫度時的溶解度。
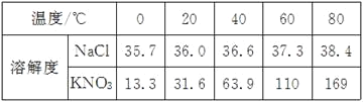
(1)若要比較KNO3與NaCl在水中的溶解能力,需要控制的變量是水的質量和________。
(2)20℃時,各取NaCl、KNO3固體3.5g分別加入10g水中,充分溶解后達到飽和狀態的是________溶液。
(3)若將上表數據在坐標系中繪制成NaCl和KNO3的溶解度曲線,兩條曲線的交點對應的溫度范圍是________(填序號)。
A 0 ℃~20 ℃ B 20 ℃~40 ℃
C 40 ℃~60 ℃ D 60 ℃~80 ℃
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請根據下列實驗裝置圖回答問題。
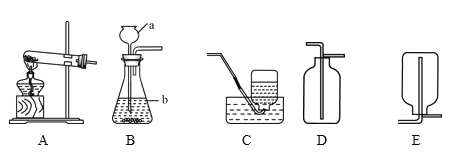
(1)寫出儀器a、b的名稱,a是__________,b是__________。
(2)若用B裝置制取二氧化碳,反應的化學方程式是__________。稀鹽酸一加入錐形瓶內立即用排水法收集滿一集氣瓶的二氧化碳,然后做蠟燭熄滅實驗,蠟燭沒有熄滅的原因是__________。
(3)實驗室用加熱氯化銨(NH4C1)和氫氧化鈣固體混合物的方法制取氨氣(NH3)同時得到氯化鈣和水。該反應的化學方程式是__________,應選用的發生裝置為__________(填裝置編號)
(4)收集氨氣時只能選用E裝置,把收集滿氨氣的集氣瓶倒扣在滴有無色酚酞試液的水 槽中,觀察到集氣瓶內有大量液體進入,并變成紅色。
根據上述信息總結出氨氣的性質有__________、__________(回答兩條即可)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據下列數型圖像回答:

(1)圖一是用鹽酸和氫氧化鈉進行中和反應時,反應過程中溶液的pH變化曲線。向鹽酸中加入的氫氧化鈉溶液質量為mg時,所得溶液中含有的離子為 (填離子符號)
(2)圖二是20℃時,取10mL10%的NaOH溶液于燒杯中,逐滴加入10%的鹽酸,隨著鹽酸的加入,燒杯中溶液溫度與加入鹽酸體積的變化關系
①由圖可知中和反應是放熱反應,你的依據為
②甲同學用氫氧化鈉固體與稀鹽酸反應也能得到相同結論,乙同學認為不嚴密,因為
(3)圖三是a、d、c三種物質的溶解度曲線。a與c的溶解度相交于P點,據圖回答:
①t1℃時,接近飽和的c物質溶液,在不改變溶液質量的條件下,可用 的方法達到飽和狀態
②將t2℃時,150g a物質的飽和溶液降溫到t1℃時。可以析出 g a物質。
(4)下圖托盤天平兩邊是等質量的鐵和鎂分別跟等質量等濃度的稀硫酸反應,反應時間t與生成氫氣質量m的變化關系如圖四。
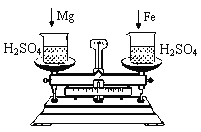
試回答:從開始反應到不再產生氣體為止,天平指針偏轉情況是
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com