
【題目】化學用語是學習化學的重要工具。
(1)寫出下列微粒的化學符號:
①人體中含量最多的物質____________;②保持氦氣化學性質的粒子____________;
③2個銨根離子_________________;④氯化鐵中鐵元素的化合價___________;
(2)用下列字母序號填空:
A.鎂 B.碳酸氫銨 C.大理石 D.明礬
①實驗室制CO2的原料是________;②可制作照明彈的是________;
③可用作化肥的是_______ ;④凈水時可使水中微小顆粒物沉降的是________。
(3)寫出下列反應的化學方程式:
①鐵絲燃燒__________;②濕法煉銅__________;
③小蘇打治療胃酸過多_______; ④研磨熟石灰與硫酸銨________。
【答案】 H2O He 2NH4+ ![]() Cl3 C A B D 3Fe+2O2
Cl3 C A B D 3Fe+2O2![]() Fe3O4 Fe+ CuSO4== Cu + FeSO4 NaHCO3+HCl ==NaCl+H2O+CO2↑ (NH4)2SO4+Ca(OH)2=CaSO4+2H2O+2NH3
Fe3O4 Fe+ CuSO4== Cu + FeSO4 NaHCO3+HCl ==NaCl+H2O+CO2↑ (NH4)2SO4+Ca(OH)2=CaSO4+2H2O+2NH3
【解析】(1)①人體中含量最多的物質是水,化學式為H2O;②分子是保持物質的化學性質的最小微粒,所以保持氦氣化學性質的粒子是He;③離子是用原子或原子團和右上角的數字加上正負號來表示,若要表示多個離子時,在離子符號的前面加上數字表示離子的個數,2個銨根離子表示為2NH4+;④氯化鐵中氯元素的化合價為-1價,根據化合價的代數和為0可求得鐵元素的化合價為+3價,故氯化鐵中鐵元素的化合價表示為![]() Cl3;
Cl3;
(2)①實驗室制CO2的原料碳酸鈣和稀鹽酸,故選C;②鎂在空氣中燃燒放出耀眼的白光,故可制作照明彈,故選A;③碳酸氫銨中含有氮元素,可用作化肥的選B;④凈水時可使水中微小顆粒物沉降的是明礬;
(3)寫出下列反應的化學方程式:
①鐵絲與氧氣反應生成四氧化三鐵,反應方程式為3Fe+2O2點燃Fe3O4;②濕法煉銅是鐵與硫酸銅反應生成銅和硫酸亞鐵,反應方程式為Fe+ CuSO4 == Cu + FeSO4 ;③小蘇打治療胃酸過多是碳酸氫鈉與稀鹽酸反應生成二氧化碳和水和氯化鈉,反應方程式為NaHCO3+HCl ==NaCl+H2O+CO2↑; ④研磨熟石灰與硫酸銨是氫氧化鈣與硫酸銨反應生成硫酸鈣
氨氣和水,反應方程式為:(NH4)2SO4+Ca(OH)2=CaSO4+2H2O+2NH3;


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
【題目】下圖是兩種元素在周期表中的信息。請回答:
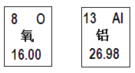
(1)氧元素的原子序數是________;氧離子的符號是________。
(2)若鋁離子的結構示意圖為:![]() ,則Y=________
,則Y=________
(3)寫出這兩種元素組成的化合物的化學式_____________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】人類社會的發展離不開金屬。請依據所學的知識填空。
(1)下列制品的用途,利用金屬導熱性的是___________。

(2)金屬資源在地球上分布廣泛。人們在自然界中僅發現金、銀等少數金屬單質,其余金屬元素都以化合物形式存在。你認為金屬的存在形式主要和______有關。
(3)農業上用硫酸銅、生石灰加水配制波爾多液作為殺菌劑。有經驗的農民都不用鐵制容器來配制或盛放波爾多液,原因是____________________________(用化學方程式表示)。
(4)在空氣中鋁制品更耐腐蝕,用化學方程式表示其原因是___________。
(5)廢舊鐵鍋、鋁鍋不要隨意丟棄,應回收利用。這樣做的意義是___________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】我國化工專家侯德榜創立了“侯氏制堿法”,促進了世界制堿技術的發展。流程簡圖如下(已知:母液中有一種銨態氮肥) ,下列有關說法不正確的是 ( )
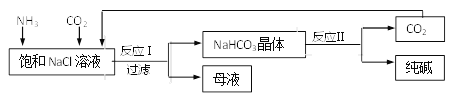
A. 反應中先通入氨氣的目的是促進二氧化碳的吸收,提高產率
B. “母液”中一定只含有兩種溶質
C. 反應II得到的CO2可以循環使用
D. 反應I的方程式為NaCl+NH3+CO2=NaHCO3↓+NH4Cl
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】鋅及其氧化物(ZnO,白色,難溶于水,溶于強酸)具有廣泛的應用。
(一)鋅的廣泛應用
(1)鋅被稱之為“生命元素”。兒童、青少年如果缺鋅嚴重,將會導致“____ 癥”和智力發育不良。經常吃貝殼類海產品、紅色肉類等含鋅的食物有利補“鋅”。這里的“鋅”是指__________。
A.單質 B.元素 C.原子 D.分子
(2)實驗室用鋅與稀硫酸制取氫氣,反應的化學方程式為__________________________。
(3)鋅與銅熔合可形成“黃銅”,它屬于______(選填序號)。
A.金屬材料 B.無機非金屬材料 C.合成材料 D.復合材料
(二)活性ZnO制取的探究
【實驗方案】工業上用粗氧化鋅(含少量FeO)制取活性氧化鋅,其流程如下:
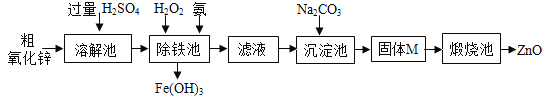
【查閱資料】一些陽離子以氫氧化物形式開始沉淀、完全沉淀時溶液的pH見下表。
沉淀物 | Fe(OH)3 | Zn(OH)2 | Fe(OH)2 |
開始沉淀pH | 1.5 | 6.2 | 6.3 |
完全沉淀pH | 3.2 | 8.0 | 9.7 |
【問題探究】
(4)“溶解”前將粗氧化鋅粉碎成細顆粒,目的是___________________。
(5)“溶解”后得到的酸性溶液中含有ZnSO4、____、FeSO4。除鐵池中加入適量H2O2,使Fe2+轉化為Fe3+;為使溶液中Fe3+全部轉化為Fe(OH)3,而Zn2+不形成Zn(OH)2,則應加入氨水控制溶液的pH的范圍為_____________。
(6)“沉淀池”中的沉淀經過濾、洗滌等操作得純凈固體M,其組成為:aZnCO3·bZn(OH)2·cH2O。
確認固體M已經洗滌干凈的操作是:取最后一次洗滌液,最好選擇下列_______,向其中滴入無現象,則已經洗干凈。
A.紫色石蕊試液 B.少量稀鹽酸 C.氯化鋇溶液或硝酸鋇溶液
【組成測定】固體B的組成會影響制得的ZnO的活性。為確定aZnCO3·bZn(OH)2·cH2O的組成,進行如下實驗(假設每步反應、吸收均完全):
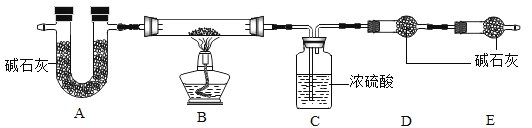
【查閱資料】aZnCO3·bZn(OH)2·cH2O受熱分解生成ZnO、H2O、CO2三種產物。
(7)寫出裝置B中發生反應的化學方程式______________________。
現稱取35.9 g aZnCO3·bZn(OH)2·cH2O在B裝置中進行完全煅燒,測得裝置C和D的質量分別增重7.2 g和4.4 g。
【實驗分析及數據處理】
(8)該實驗反應前后均需要通入空氣,反應后通入空氣的目的是_______。
(9)裝置A的作用是__________________。
(10)根據上述數據,則生成ZnO的質量為______g;a:b:c=________。
(11)若沒有E裝置,則測得的a值________(填“偏大”、“ 偏小”或“不變”)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】數十年來,化學工作者對碳的氧化物和氫化物做了廣泛深入的研究并取得了一些重要成果。
(1)工業上常采用將水蒸氣噴到灼熱的炭層上實現煤的氣化(制得CO、H2),該反應的化學方程式是_______,制得的CO是一種有毒氣體,能降低_________的攜氧能力。
(2)上述煤氣化過程中需向炭層交替噴入空氣和水蒸氣,噴入空氣的目的是________;氣化得到的氣體可在加熱和催化劑下合成液體燃料甲醇CH3OH,該反應方程式為
________________________________________。
(3)科學家用氮化鎵材料與銅組裝如圖的人工光合系統,利用該裝置成功地實現了以CO2和H2O合成CH4。
①寫出合成甲烷的化學方程式_________。
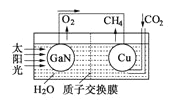
②為提高該人工光合系統的工作效率,可向裝置中加入少量的_______(選填“氫氧化鈉”或“硫酸”)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】有關金屬的性質。
I. 把一定質量的鋅粉投入到硫酸亞鐵和硫酸銅的混合溶液A中,充分攪拌,過濾。回答下列問題。
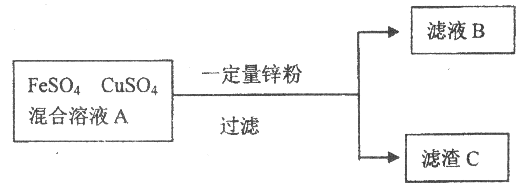
(1)若向濾渣C中加入適量稀硫酸,有氣體生成。濾渣C中一定有____________,濾液B中除水外,一定有___________。
(2)若向溶液A中加入過量的鋅粉,寫出向濾渣C中加入足量硫酸,發生的反應的化學方程式為__________________。
II. 為了驗證金屬活動性強弱和驗證質量守恒定律,同學們設計了如圖所示的實驗。
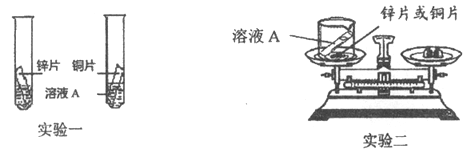
(1)利用實驗一和實驗二,既能驗證銅、鋅金屬活動性強弱,同時能驗證質量守恒定律,則溶液A可以是_________(填序號)。
a. 稀硫酸 b. 硝酸銀溶液 c. 氯化亞鐵溶液 d. 硫酸鋅溶液 e. 硫酸銅溶液
(2)利用以上試劑設計反應,驗證銅和銀的金屬活動性,化學反應方程式為_________,現象為_________。
III. 某同學為了探究鐵釘生銹條件,設計了如下實驗。
序號 | ① | ② | ③ | ④ |
實驗內容 |
|
|
|
|
實驗現象 | 鐵釘無明顯變化 | 鐵釘生銹 | 鐵釘無明顯變化 | 鐵釘生銹 |
(1)通過實驗①、②對比得出的結論是_________。
(2)實驗④中,一段時間后,觀察到U型管左側液面_________(填“上升”、“不變”或“下降”),原因是_________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】化學興趣小組同學發現實驗臺上按如圖所示順序擺放著6瓶不同的無色溶液(如圖所示:A、B、C、D、E、F代表對應的溶液)。其中E溶液的試劑瓶標簽破損.為此,他們做了如下探究:
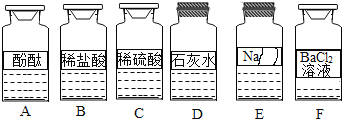
【提出問題】E溶液的成分是什么?
【初步判斷】根據受損標簽及實驗室藥品分類擺放原則,E溶液不可能是_______(填序號)①酸;②堿;③鹽。
【提出猜想】
猜想Ⅰ:NaOH溶液;
猜想Ⅱ:Na2CO3溶液;
猜想Ⅲ:Na2SO4溶液;猜想Ⅳ:____溶液(任寫一種).
設計并實驗興趣小組的同學為驗證“猜想Ⅱ”是否正確,設計并完成如下表所示實驗。
實驗方案 | 實驗一 | 實驗二 | 實驗三 |
實驗操作 |
|
|
|
實驗現象 | 試紙變色,對照比色卡,pH>7 | 有無色無味氣體產生 | _____________ |
實驗結論 | 猜想Ⅱ正確 | ||
【分析與推理】
①完成“實驗一”后,李成同學即認為“猜想Ⅰ”正確,張平同學認為“猜想Ⅰ”不一定正確,他的理由是_________________________。
②請寫出“實驗三”中發生反應的化學方程式___________________________。
【反思與評價】
經過討論,同學們認為實驗中存在明顯操作錯誤,該錯誤是___________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室有一份碳酸鈉和硫酸鈉的混合粉末,為測定其中碳酸鈉和硫酸鈉的質量比,小冰做了如圖所示的實驗:
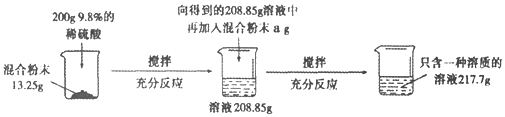
請回答下列問題:
(1)上述實驗過程中發生反應的化學方程式為____________________________;
(2)向13.25g樣品中加入200g稀硫酸后,生成氣體的質量為_______________;
(3)根據已知條件,列出求解與13.25g樣品反應的稀硫酸中溶質質量(x)的比例式________________;
(4)a的數值是_________;
(5)混合粉末中碳酸鈉和硫酸鈉的質量比為_________;
(6)若要使最終所得溶液溶質的質量分數變為10%,則需要向其中加入水的質量為____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com