
【題目】已知A、B、C、D是本學期化學學習中常見的四種物質,轉化與反應關系如圖,A與B在一定條件下反應生成C和D,C在一定條件下可轉化為A。
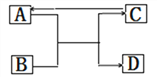
(1)如果A、C的組成元素相同,D為紫紅色金屬單質。則B的化學式為________,C轉化為A的反應屬于______________反應。
(2)如果A、B、C常溫下無為氣體,B是天然氣的主要成分,寫出D物質的一種用途___________,寫出圖中A與B反應的化學方程式__________________。
【答案】 CuO 化合 用于溶解物質(或用于加熱或冷卻或配制試劑等) CH4 + 2O2 ![]() CO2 + 2H2O
CO2 + 2H2O
【解析】(1)D為紫紅色金屬單質,所以D為銅,又因為A、C的組成元素相同,A與B在一定條件下反應生成C和D;則高溫條件下,氧化銅和一氧化碳反應生成銅和二氧化碳,二氧化碳和碳反應生成一氧化碳,因此ABCD分別是一氧化碳、氧化銅、二氧化碳和銅;氧化銅化學式為CuO;二氧化碳和碳在高溫下反應生成一氧化碳,化學方程式為:CO2+C ![]() CO,符合“多變一”的特點,屬于化合反應;
CO,符合“多變一”的特點,屬于化合反應;
(2)B是天然氣的主要成分,所以B為甲烷,甲烷燃燒生成水和二氧化碳,所以ABCD分別是氧氣、甲烷、二氧化碳和水;水可以用于溶解物質或用于加熱或冷卻或配制試劑等;甲烷在氧氣中燃燒生成水和二氧化碳,化學方程式為CH4 + 2O2 ![]() CO2 + 2H2O。
CO2 + 2H2O。


 輕松奪冠全能掌控卷系列答案
輕松奪冠全能掌控卷系列答案科目:初中化學 來源: 題型:
【題目】元素家族新成員——鉨(![]() )
)
2016年6月8日,國際純粹與應用化學聯合會正式發布113號等四種新元素的英文名稱和元素符號。2017年5月9日,我國發布了這四種元素的中文名稱。其中113號元素的元素符號為Nh,中文名稱為“鉨”。圖1中,甲為鉨原子結構示意圖,乙為鋁原子結構示意圖。請回答下列問題;
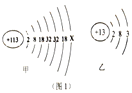
(1)甲中x=________。
(2)鉨元素的原子與鋁元素的原子具有相同的_____________數。
(3)在化學反應中,鉨原子形成離子的符號為___________。
(4)根據鉨和鋁的結構,理論上鉨的金屬活動性比鋁強,試預測鉨可能與哪些物質反應? ________,________。(寫出兩種不同類別的物質的化學式即可)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】化學研究物質的組成、結構、性質和變化規律。請回答:
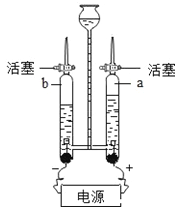
①如圖所示裝置可以研究水的組成,反應的化學方程式是______________________,a處氣體可以用________________檢驗。
②有四種微粒的微觀示意圖如下,其中能構成單質的是_______________。
![]()
③某興趣小組同學通過以下實驗研究活性炭的吸附性(活性炭是一種難溶于水的黑色粉末):
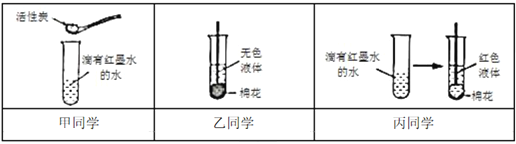
I.甲同學:在一支試管中加入約5mL的水,滴加1-2滴紅墨水,往試管中加少量活性炭,振蕩,發現活性炭懸浮于液體中,未能觀察到預計的實驗現象。
II.乙同學:在甲同學的基礎上,用玻璃棒將一團棉花從試管口慢慢推推入底部(如上圖),請問此處棉花的作用__________________________。
III.丙同學:丙同學認為乙同學的實驗還不能達到實驗目的,又增加了一個對比實驗,請問丙同學實驗的目的是什么_____________________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
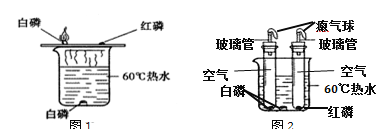
【題目】(1)下圖1裝置是對“可燃物燃燒的條件”進行探究。圖2是某小組的改進裝置,這樣改進的優點是___;改進試驗中試管中白磷燃燒而熱水中白磷沒有燃燒,說明燃燒需要的條件是____。
(2)用二氧化碳滅火器(如下圖)滅火時,手一定要握在鋼瓶的木柄上,以免凍傷。由此可知二氧化碳滅火器的滅火原理是______________________。

查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請將下列短文中帶點的部分,用恰當的化學用語填寫在橫線上:
太陽鏡具有保護眼睛的功能。玻璃鏡片的主要成分是二氧化硅__________,且變色玻璃中含有銀離子__________,銅制鏡框使用時間過長會生成銅綠[Cu2(OH)2CO3],銅綠中碳元素的化合價顯+4價________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下表所示各組物質中,物質之間按箭頭方向通過一步反應就能實現如下圖所示轉化的是( ) 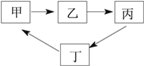
物質 選項 | 甲 | 乙 | 丙 | 丁 |
A | CO2 | CaCO3 | H2O | O2 |
B | KOH | KCl | CO2 | K2CO3 |
C | H2O2 | H2O | O2 | MgO |
D | CaO | Ca(OH)2 | H2O | CaCl2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】以下是兩個常見的工業流程,

流程一:從只含有CuSO4的廢液中回收金屬銅,并得到工業原料硫酸亞鐵,生產流程如下:
(1)加入過量的A物質,該A物質為______。操作a的名稱是 _______,操作a所用到的玻璃儀器有燒杯、玻璃棒、_________,操作a中玻璃棒的作用是 _______ 。
(2)寫出流程圖中的固體成分的化學式 ____ ,B的溶液中溶質的化學式 _______
流程二:如圖是兩種常用脫硫工藝中含硫物質的轉化路徑(部分產物已略),請回答下列問題:
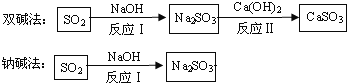
(1)CaSO3中Ca、S、O元素的質量比是_______。
(2)已知原料NaOH的價格為2.9元/kg. 而Ca(OH)2的價格為0.36元/kg.兩種工藝中,處理相同質量的SO2,雙堿法所需的原料成本更低,其原因是______________。
【答案】 鐵 過濾 漏斗 引流 Fe和Cu H2SO4 5:4 : 6 雙堿法中通過反應II實現了NaOH的循環利用,減少了NaOH的用量 處理等量SO2,氫氧化鈣用量更少且價格便宜,所以雙堿法成本更低
【解析】流程一:只含有CuSO4的廢液中回收金屬銅,并得到工業原料硫酸亞鐵,所所加試劑是過量的鐵,反應方程式為Fe+CuSO4==FeSO4+Cu ,反應后得到是固體銅和鐵,溶液硫酸亞鐵溶液,過濾可將難溶固體與液體分離,所以應過濾,過濾用到的儀器有:燒杯、漏斗、玻璃棒、鐵架臺,其中,玻璃棒的作用是引流;將銅和鐵的混合物中的鐵除掉,得硫酸亞鐵和銅,所以應加入的試劑B為稀硫酸,因為.Fe+H2SO4=FeSO4+H2↑,而銅和酸不反應;流程二:(1)化合物中元素的質量比=(相對原子質量×原子個數)之比,CaSO3中Ca、S、O元素的質量比是40:32:3×16= 5:4 : 6;(2)Na2SO3 + Ca(OH)2 = CaSO3↓+2NaOH , 2NaOH+ SO2 == Na2SO3+ H2O;因此用雙堿法(氫氧化鈣和氫氧化鈉聯合使用)實現了NaOH的循環利用,減少了NaOH的用量 處理等量SO2,氫氧化鈣用量更少且價格便宜,所以雙堿法成本更低。
【題型】流程題
【結束】
26
【題目】堿式碳酸鎂密度小,是橡膠制品的優良填料。其組成一般以xMgCO3·yMg(OH)2·zH2O表示。
【探究一】堿式碳酸鎂的制備
堿式碳酸鎂可用復鹽MgCO3·(NH4)2CO3·H2O作原料制備。取一定量的該復鹽放入三頸燒瓶中,并將三頸燒瓶放在恒溫水浴鍋中加熱(如下圖所示),按一定的液固比加入蒸餾水,開啟攪拌器同時加入預定的氨水,待溫度到達 40℃時開始分解,此時滴加鹵水(氯化鎂溶液)并繼續滴入氨水,保持10分鐘,一段時間后過濾洗滌,濾出的固體在120 ℃干燥得到堿式碳酸鎂產品。
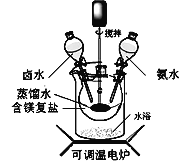
回答下列問題:
(1)攪拌的目的是________。
(2)設計實驗檢驗堿式碳酸鎂中含有Cl-
實驗操作 | 實驗現象 | 實驗結論 |
①取樣溶解,向樣品溶液中滴加過量稀硝酸。 ②再向上述所得溶液加____溶液 | 現象①____; 現象②____; | 含有 Cl- |
【探究二】探究小組利用下圖測定xMgCO3·yMg(OH)2·zH2O組成。已知:
(1)堿石灰的主要成分為氫氧化鈉和生石灰,能吸收水蒸氣和二氧化碳;
(2)堿式碳酸鎂分解反應方程式為:xMgCO3·yMg(OH)2·zH2O === (x+y)MgO + xCO2↑+ (y+z) H2O
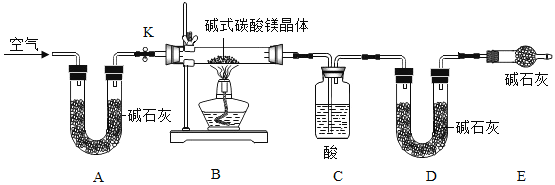
實驗步驟:
步驟1:檢查裝置的氣密性,將過濾、洗滌并干燥過的樣品置于平直玻璃管中。
步驟2:打開活塞K,鼓入空氣,一段時間后關閉,稱量相關裝置的質量。
步驟3:加熱裝置B直至裝置C中無氣泡產生。
步驟4:______(請補充該步操作內容)。
步驟5:稱量相關裝置的質量。
某同學在實驗過程中采集了如下數據:
A.反應前玻璃管的質量100.0 g B.反應后玻璃管與殘留固體總質量120.0 g
C.裝置C實驗后增重9.0 g D.裝置D實驗后增重17.6 g
回答下列問題:
(1)檢查整套實驗裝置氣密性:將裝置A的左端、裝置E的右端分別接上導管,放入盛有水的燒杯中,打開活塞K,對裝置B用酒精燈微熱,若觀察到____,則氣密性良好;
(2)裝置A的作用是____,如果沒有裝置A,則測定得到xMgCO3·yMg(OH)2·zH2O中的z值____(填“偏大”、“偏小”、“無影響”),裝置C中的酸為___(寫名稱);
(3)根據實驗測定的數據,求出堿式碳酸銅(xMgCO3·yMg(OH)2·zH2O)中x∶y∶z的最簡整數比是_(要求寫出過程)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】廢舊金屬可以回收利用,用合金廢料(含Fe、Cu和Al)制取FeSO4和CuSO4溶液的實驗流程如圖(部分生成物已略):

(1)合金屬于 (填“純凈物”或“混合物”);
(2)步驟①反應的化學方程式為:2Al+2NaOH+2R═2NaAlO2+3H2↑,依據質量守恒定律推出R的化學式為 ,步驟②反應的化學方程式為 ;
(3)由Cu制取CuSO4溶液有以下三種途徑:
I.Cu+2H2SO4(濃)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
Ⅱ.2Cu+O2![]() 2CuO CuO+H2SO4═CuSO4+H2O
2CuO CuO+H2SO4═CuSO4+H2O
Ⅲ.3Cu+8HNO3═3Cu(NO3)+2NO↑+4H2O
你認為最佳途徑是 (填序號),理由是 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】水是寶貴的自然資源,對于人類生活、生產都具有重要意義。
(1)水的組成
有關水的組成和結構的敘述中,正確的是____________________________(填字母);
A.水中氫、氧元素的質量比為2 :1 B.水是由水分子構成的
C.水分子是由氫分子和氧原子構成的 D.保持水的化學性質的最小微粒是氫原子和氧原子
(2)水的性質
① 少量下列物質加入到水中,充分攪拌后,可以得到溶液的是_______________________。
A.牛奶 B.蔗糖 C.面粉 D.花生油
② 實驗室中用5g氯化鈉配成溶質質量分數為10%的氯化鈉溶液,則需加入蒸餾水___________mL,所配溶液質量分數偏小的原因可能是___________________________。(填一種即可)
③ 甲、乙、丙三種不含結晶水的固體物質的溶解度曲線如下圖。下列說法不正確的是_________。

A.t1℃時,三種物質的溶解度:乙>甲=丙
B.20℃時,將30g甲放入50g水中,充分攪拌,所得溶液的質量是70g
C.分別將t2℃時三種物質的飽和溶液降溫到t1℃,甲溶液中析出的晶體質量最大
D.t2℃時將相同質量的甲、乙、丙三種物質分別加入到100g水中充分溶解后,若只有一種固體物質沒有完全溶解,則該固體一定是丙
(3)水的用途
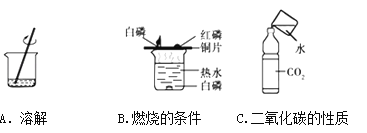
①實驗A中水作______________________(填“溶劑”或“溶質”)。
②實驗B中水的作用是提供熱量和____________________。
③實驗C中的水作_______________________________。
④滅火時將水噴成細霧狀的主要原因是______________________(選填編號)。
A.降低著火點 B.增大與可燃物接觸面積 C.與空氣中氣體反應生成CO2D.隔離氧氣
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com