
【題目】下列圖像能正確反映其對應關系的是
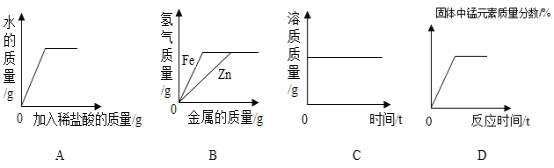
A. 向一定量的氫氧化鈉溶液中逐滴加入稀鹽酸至過量
B. 向兩份完全相同的稀硫酸中分別加人足量鋅粉、鐵粉
C. 某溫度時,向一定量的飽和石灰水中加入少量生石灰再恢復至原溫
D. 加熱一定質量的高錳酸鉀制取氧氣
【答案】B
【解析】
A、氫氧化鈉和鹽酸反應生成氯化鈉和水,水的質量不能從零開始,故錯誤;
B、等質量的鐵和鋅與酸反應,鐵生成的氫氣多,相同的酸與金屬反應生成的氫氣的質量相同,故正確;
C、因為開始生石灰與水反應生成氫氧化鈣,所以溶劑質量減少,對于飽和氫氧化鈣溶液來說,溶劑減少就會析出溶質,所以溶質減少,由于生石灰與水反應生成氫氧化鈣時放出熱量,在反應過程中溫度升高,溶解度減小,但冷卻后溫度降低,溶解度又增大了,又溶解了一部分,溫度不變后溶質也不變了,故錯誤;
D、高錳酸鉀在加熱的條件下分解為錳酸鉀、二氧化錳和氧氣,隨著反應的進行,固體質量減少,而由質量守恒定律可知,固體中錳元素的質量不變(即錳元素質量分數不為零),所以隨著反應的進行固體中錳元素的質量分數增大,直到高錳酸鉀完全分解為止,故錯誤。
故選C。


 科學實驗活動冊系列答案
科學實驗活動冊系列答案科目:初中化學 來源: 題型:
【題目】某粗鹽中除NaCl以外還含有少量雜質MgCl2,為了測定粗鹽中MgCl2的質量分數。取固體樣品50.0g完全溶解于150.0g水中,并向其中逐漸加入一定濃度的NaOH溶液,實驗過程中生成沉淀的質量與加入NaOH溶液的質量的關系如圖所示:

注:發生反應的化學方程式為:MgCl2+2NaOH=Mg(OH)2↓+2NaCl
請根據相關信息完成下列計算:
(1)反應完全時,生成氫氧化鎂的質量為_____g;
(2)在粗鹽中氯化鎂的質量分數;_____
(3)恰好完全反應時得到的溶液中溶質的質量分數。_____
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】已知A、B、C三種物質含有同種金屬元素,其中A是大理石的主要成分,B為氧化物;D、E、F 三種物質含有同種非金屬元素,其中E與血紅蛋白的結合力大約是氧氣的200~300倍,F是單質。將A高溫煅燒,得到B與D,它們之間的轉化關系如圖所示(有些轉換關系,反應條件等略去),試回答:
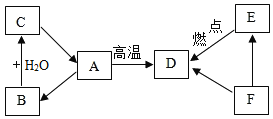
(1)B的化學式為_____;
(2)C在工農業生產、生活中的主要用途有(寫出一條)_____;
(3)D+F→E的化學方程式:_____,此反應的類型為_____;
(4)正是因為大氣中有D等氣體的存在所引起的_____,使得全球平均地表溫度提高到適合人類生存的15℃。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖是某化學興趣小組。設計的金屬活動性順序的探究實驗。
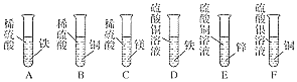
(1)上述實驗中,有氣泡生成的是________(填寫裝置序號)。
(2)試管F中出現的實驗現象是______________。
(3)上述實驗能否證明鎂、鋅、鐵、銅、銀五種金屬的活動性強弱?____請說明理由_____。
(4)我國古代“濕法煉銅”就是利用了試管D中的反應原理,請寫出該反應的化學方程式:______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在“氧氣的制取和性質”實驗中,某同學取一段紗窗網上還能任意彎曲的細鐵絲,在新制的氧氣中做“鐵絲燃燒”的實驗。結果沒有觀察到“火星四射”的現象,請分析此實驗失敗的可能原因: (寫一種);經過改進后實驗成功了,其反應的文字表達式 。實驗時要在集氣瓶底部鋪一層細沙或裝少量水的原因是 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】把A、B、C、D四種物質放在密閉容器中,在一定條件下充分反應,并測得反應物和產物在反應前后各物質的質量如表所示:
物質 | A | B | C | D |
反應前質量 |
|
|
|
|
反應后質量 | 待測 |
| 0 |
|
下列說法正確的是![]()
A. 物質C一定是反應物,物質D可能是單質
B. 反應后密閉容器中A的質量為![]()
C. 反應過程中,物質B和物質D變化的質量比為87:36
D. 若物質A與物質C的相對分子質量之比為194:216,則反應中A和C的化學計量數之比為2:1
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】2009年邵陽市九年級化學實驗操作技能考試中,小聰同學抽到的試題是“探究酸和堿之間的中和反應“。他向盛有氫氧化鈉溶液的燒杯中緩慢滴加稀鹽酸,一會兒后,想起忘記加指示劑了,便補加幾滴無色酚酞溶液,攪拌,觀察到溶液不變色,于是他得出“酸堿恰好完全中和”的結論。
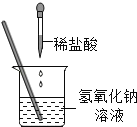
(1)該中和反應的化學方程式是_____;
(2)老師給予小聰的評定是結論不準確。請你幫小聰分析老師的理由是:_____
(3)請你另外設計一個實驗,探究小聰實驗后燒杯中的溶液是否“恰好完全中和”。
填寫下表:
實驗步驟 | 實驗現象 | 實驗結論 |
_____ | _____ | _____ |
_____ | _____ |
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某化學小組利用如圖所示裝置(圖中固定裝置已略去)測定銅鋅合金中鋅的質量分數,探究過程如下:
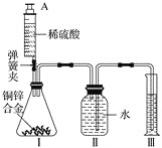
①連接實驗裝置并檢查裝置氣密性。
②向裝置Ⅰ中的錐形瓶加入2.0g的銅鋅合金樣品粉末,由注射器緩緩注入稀硫酸,待到錐形瓶中不再產生氣體時,準確讀取注射器內讀數,減少10.5mL稀硫酸,同時立即夾緊彈簧夾,移出裝置Ⅲ中的導管,準確讀取量筒內水的體積為214.0mL(注:樣品中的雜質不參加反應
③裝置Ⅰ中剩余固體物質經過適當處理后,準確稱量其質量為1.4g
④該小組的三位同學利用實驗過程測得不同數據,計算銅鋅合金樣品中鋅的質量分數
甲同學利用裝置Ⅰ中反應前后固體的質量進行計算;
乙同學利用裝置Ⅰ中加入稀硫酸的量進行計算;
丙同學利用裝置Ⅲ中量取水的體積進行計算,并查得:在標準狀況下,氫氣的密度為0.09gL-1。
回答下列問題:
(1)裝置Ⅰ中反應的化學方程式為___,實驗過程中須加入稀硫酸至不再產生氣體,目的是___。
(2)步驟③中稱量剩余固體之前的正確操作是_______、洗滌、干燥。
(3)根據實驗測定的數據,上述三位同學中________(填“甲”、“乙”或“丙”)同學無法進行計算樣品中鋅的質量分數。
(4)化學小組同學發現:按照丙同學的方案進行計算,致使實驗結果出現較大偏差。以下因素可能造成偏差的有________(填標號)。
A 移出裝置Ⅲ時,導管內留存了一部分水
B 實驗測量前,沒有排除裝置Ⅰ中的空氣
C 數據處理時,未排除加入稀硫酸所占的體積
【答案】(1)![]() ;使樣品中的鋅完全反應;(2)過濾;(3)乙;(4)AC;
;使樣品中的鋅完全反應;(2)過濾;(3)乙;(4)AC;
【解析】
試題(1)由于銅排在了氫的后面,所以與酸不反應,反應物是鋅和硫酸,生成物是硫酸鋅和氫氣,氫氣后面標上上升符號;實驗過程中須加入稀硫酸至不再產生氣體,目的是使樣品中的鋅完全反應;(2)從銅和硫酸鋅溶液的混合物中得到銅,先進行過濾,得到帶有硫酸鋅溶液的銅,再進行洗滌除去表面的硫酸鋅,再進行干燥除去水即可;(3)根據加入稀硫酸的量進行計算需要知道稀硫酸的溶質質量分數,而題中沒有告知;(4)由于鋅與硫酸反應生成硫酸鋅和氫氣時,放出熱量,如果沒等冷卻到室溫,根據熱漲冷縮的原理可知進入量筒中水偏多,所以誤認為得到的氫氣多,再就是數據處理時,未排除加入稀硫酸所占的體積,計算的結果就偏大;
考點:金屬的化學性質;化學方程式;實驗誤差分析;
點評:熟記金屬活動性順序表,知道排在氫之前的金屬和稀鹽酸或者硫酸反應生成氫氣,而排中氫之后的金屬和稀鹽酸或者稀硫酸不生成氫氣;化學反應中物質的質量比都是純凈物之間的質量比,而溶液中溶質的質量=溶液質量×溶質質量分數;本題容易出錯的地方是對實驗結果的評價,要知道鋅與硫酸反應放出熱量,會造成相應的誤差,必須冷卻到室溫才能進行觀察和計算。
【題型】實驗題
【結束】
30
【題目】用1000t含氧化鐵80%的赤鐵礦石,理論上可以煉出含鐵96%的生鐵的質量是多少?
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com