
【題目】西藏“茶馬古道”芒康縣鹽井是香格里拉唯一的產鹽區。鹽田是用紫紅色粘土抹平壓實的曬鹽池,當地人把鹵水注入鹽田中經過日曬風吹,就得到上等且味道很好的紅鹽。為揭密紅鹽呈紅色的原因,實驗小組進行了如下探究活動。
(提出問題)紅鹽中存在什么物質使鹽呈現紅色?
(查找資料)
1、西藏紫紅色粘土中含大量的氧化鐵(Fe2O3)。
2、溶液中三價鐵離子(Fe3+)遇到硫氰化鉀(KSCN)溶液,溶液變為血紅色。
(作出猜想)紅鹽中含少量的氧化鐵使鹽呈現紅色;
(實驗探究)小組同學從一定量的紅鹽中提取少量紅色粉末,進行如下實驗:
實驗操作 | 實驗現象 | 實驗解釋與結論 | |
實驗I | 步驟①:取少量紅色粉末于試管中,滴加適量稀鹽酸; | 紅色粉末恰好全部溶解; | 紅色粉末中含有_____;步驟①涉及的反應的化學方程式_____ |
步驟②:往①所得溶液中滴入硫氰化鉀(KSCN)溶液。 | 溶液變為血紅色 | ||
實驗Ⅱ | 步驟①:如圖所示,將紅色粉末與足量的黑色炭粉混合均勻,裝入玻璃管中,先通一段時間氮氣,再加熱。
| 一定時間后,觀察到澄清石灰水變渾濁,紅色粉末變黑色 | 反應產生的氣體為_____;紅色粉末中一定含_____元素 |
步驟②:冷卻后,取出玻璃管中黑色粉末,將磁鐵靠近黑色粉末 | 黑色粉末部分被吸引 | 紅色粉末中一定含_____元素 |
(實驗結論)猜想_____(填寫“正確”或“錯誤”)。
(實驗反思)實驗Ⅱ中能否用CO氣體代替黑色炭粉并說明理由_____。
【答案】Fe3+(或鐵離子)或Fe2O3(或氧化鐵) Fe2O3+6HCl=2FeCl3+3H2O CO2 氧(或O) 鐵(或Fe) 正確 不能,一氧化碳中含氧元素,無法判斷紅色粉末中是否含氧元素
【解析】
[實驗探究]實驗Ⅰ:步驟①:取少量紅色粉末于試管中,滴加適量稀鹽酸,紅色粉末恰好全部溶解;步驟②:往①所得溶液中滴入硫氰化鉀(KSCN)溶液,溶液變為血紅色。說明紅色粉末中含有氧化鐵;步驟①涉及的反應是氧化鐵和稀鹽酸反應生成氯化鐵和水,反應的化學方程式為:Fe2O3+6HCl=2FeCl3+3H2O;
實驗Ⅱ:步驟①:如圖所示,將紅色粉末與足量的黑色炭粉混合均勻,裝入玻璃管中,先通一段時間氮氣,再加熱,一定時間后,觀察到澄清石灰水變渾濁,紅色粉末變黑色,說明反應生成了二氧化碳,進一步說明紅色粉末中一定含氧元素;
步驟②:冷卻后,取出玻璃管中黑色粉末,將磁鐵靠近黑色粉末,黑色粉末部分被吸引,說明生成物中含有鐵,進一步說明紅色粉末中一定含鐵元素;
[實驗結論]由實驗探究可知,猜想正確;
[實驗反思] 實驗Ⅱ中不能用CO氣體代替黑色炭粉,因為一氧化碳中含有氧元素,無法判斷紅色粉末是否含有氧元素。


 A加金題 系列答案
A加金題 系列答案 全優測試卷系列答案
全優測試卷系列答案科目:初中化學 來源: 題型:
【題目】二維價類圖可有效幫助我們建立物質之間的聯系,高效進行化學學習。
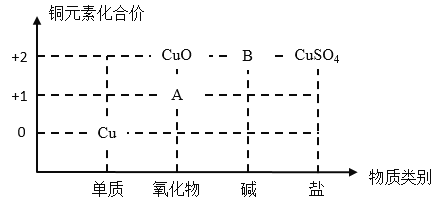
(1)銅單質常用作制電線,這體現了銅的_____性;區分鐵絲和銅絲,最簡單的方法是_____。
(2)圖中物質A的化學式為_____;高溫條件下,氧化銅會分解為A和一種常見的氣體,寫出該反應的化學方程式_____。
(3)圖中物質B的化學式為_____,顏色為_____色。CuO可否通過一步反應,轉化為CuSO4_____(填“能”或“不能”)。寫出一種相對分子質量與B相等的酸與B反應的化學方程式_____,屬于_____(填基本反應類型)。
(4)常用無水硫酸銅粉末檢驗水蒸氣,該過程發生的是_____(填“物理變化”或“化學變化”)。
(5)實驗室中經常用碳酸鈉溶液與硫酸銅溶液制備產品——堿式碳酸銅,反應為:2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3↓+2_____+CO2↑。反應時若有少量3Cu(OH)2·CuCO3生成,則產品中銅元素的質量分數_____。(填“偏大”“不變”或“偏小”)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】小明是個愛學習的學生,學了化學后他梳理了以下知識:
①加熱煮沸可以降低開水的硬度;
②某粒子的結構示意圖為 ,該粒子一定是氖原子;
,該粒子一定是氖原子;
③為探究碳酸氫銨的熱穩定性,將它進行點燃實驗;
④進入溶洞先要做燈火試驗,因為二氧化碳具有毒性;
⑤為觀察金屬鎂的顏色,用砂紙打磨鎂條;
⑥滴瓶上的滴管使用過后不需清洗,直接放回原瓶。
其中正確的是( )
A.①③⑤⑥B.②③④⑤C.①⑤⑥D.①④⑤
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】現有Mg、C、O2、CO2、Cu(OH)2、H2SO4、Na2CO3、Ca(OH)2 8種物質,選用這8種物質作反應物,按下列要求寫出有關的化學反應方程式.
(1)吸熱的化合反應:__;
(2)放熱的置換反應:__;
(3)需要加熱的分解反應:__;
(4)有堿生成的復分解反應:__.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖是甲、乙兩種固體物質的溶解度曲線。
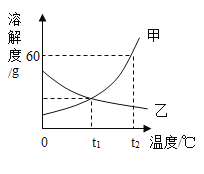
(1)在溫度為_____℃時,甲、乙兩種物質的溶解度相等;
(2)甲、乙兩物質中,通過升溫的方法能將接近飽和的溶液變為飽和溶液的是_____;
(3)t2℃時,將8g甲物質投入到10g水中,充分溶解后得到甲溶液的溶質質量分數為_____;
(4)用一定的方法將乙的不飽和溶液變為飽和溶液,下列說法正確的是_____。
A溶劑的質量可能不變 B溶質質量分數一定變大
C溶液的質量一定不變 D溶質的質量一定變大
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】發展利用太陽能可以推進節能減排。晶體硅是制造太陽能電池板的重要原料。下圖是工業上以石英砂(SiO2)為主要原料制取純硅的一種方法,請回答下列問題:(備注:粗硅中的主要成分是硅)

(1)將石英砂粉碎的目的是__________________。
(2)焦炭在反應①中體現的化學性質是______________________。
(3)寫出圖中一種氧化物的名稱___________。
(4)寫出步驟②中發生反應的化學方程式_________________________。
(5)副產品CO直接排放會污染空氣,工業上可以將之回收用來______________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】研究性學習小組選擇“H2O2生成O2的快慢與什么因素有關”的課題進行研究,以下是他們探究的主要過程:
(假設)H2O2生成O2的快慢與催化劑種類有關
(實驗方案)常溫下,在兩瓶相同體積的H2O2溶液中分別加入相同質量MnO2和紅磚粉,測量各生成一瓶(相同體積)O2所需要的時間.
(進行實驗)如圖是他們進行實驗的裝置圖,氣體發生裝置中A儀器名稱是:_____,此實驗中B處宜采用的氣體收集方法是:_____.

(實驗記錄)
實驗編號 | 1 | 2 |
反應物 | 6% H2O2 | 6% H2O2 |
催化劑 | 1g紅磚粉 | 1g MnO2 |
時間 | 152s | 35s |
(結論)該探究過程得出的結論是_____.
(反思)H2O2在常溫下分解緩慢,加入MnO2或紅磚粉后反應明顯加快,若要證明MnO2或紅磚粉是該反應的催化劑,還需要增加實驗來驗證它們在化學反應前后的_____和_____是否改變.
H2O2生成O2的快慢還與哪些因素有關?請你幫助他們繼續探究.(只要求提出假設和實驗方案)
(假設)_____.
(實驗方案)_____.
你若還能提出新的合理的假設和實驗方案。
(假設)_____.
(實驗方案)_____.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】研究表明噴灑過氧乙酸(C2H4O3)消毒液可有效滅活病毒,此消毒液屬高效消毒劑,其高濃度屬于易爆品。過氧乙酸消毒液一般市售濃度在20%,生活中需要稀釋后才能使用。下列說法正確的是
A.過氧乙酸消毒液屬于有機化合物
B.過氧乙酸完全燃燒生成二氧化碳和水
C.每個過氧乙酸由9個原子構成
D.過氧乙酸中氫元素質量分數最大
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】用如下圖所示裝置分別進行以下實驗。
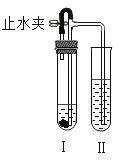
(1)打開止水夾,向Ⅰ中液體加入一種黑色固體、Ⅱ中液體加入白磷。Ⅰ和Ⅱ中均有氣泡出現,且Ⅱ中白磷燃燒。
①寫出Ⅰ中反應的化學方程式_______________________________。
②Ⅱ中白磷燃燒的原因是___________________________________。
(2)打開止水夾,向Ⅰ中稀硫酸加入少量碳酸鈉固體。Ⅰ和Ⅱ中均有氣泡出現,但Ⅱ中盛有的氫氧化鈉溶液無其它明顯現象。一段時間后,關閉止水夾,發現Ⅱ中液面上升,并產生氣泡。
①關閉止水夾前,Ⅱ中發生反應的化學方程式為_________________________。
②上述實驗能否證明二氧化碳與氫氧化鈉發生反應,理由是_____________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com