
科目: 來源: 題型:
【題目】鋁是重要的金屬材料,鋁土礦(主要成分是Al2O3和少量的SiO2、Fe2O3雜質)是工業上制取鋁的原料。實驗室模擬工業上以鋁土礦為原料制取Al2(SO4)3和銨明礬晶體[NH4Al(SO4)2·12H2O]的工藝流程如圖所示:(已知氫氧化鋁能溶解在氫氧化鈉溶液中,生成偏鋁酸鈉NaAlO2)
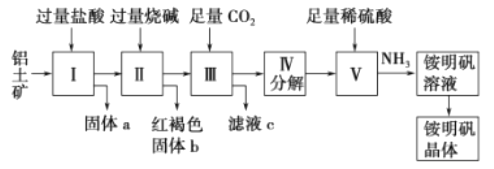
請回答下列問題:
(1)固體a的化學式為_____,Ⅲ中通入足量CO2氣體能生成氫氧化鋁和一種酸式鹽。寫出發生反應的化學方程式為_____。
(2)IV步分解指加熱使氫氧化鋁分解為相應的氧化物。由V制取銨明礬溶液的化學方程式為_____,從銨明礬溶液中獲得銨明礬晶體的實驗操作依次為(填操作名稱)_____、冷卻結晶、過濾洗滌。
(3)以1000kg含氧化鋁30.6%的鋁土礦為原料制取Al2(SO4)3,需消耗含溶質質量為_____g的98%的濃硫酸(密度1.84g·cm-1)。
(4)若同時制取銨明礬和硫酸鋁,通過控制硫酸的用量調節兩種產品的產量。若欲使制得的銨明礬和硫酸鋁的“微粒”個數之比為1:1,則投料時鋁土礦中的AI2O3和H2SO4的“微粒”個數之比為_____。
查看答案和解析>>
科目: 來源: 題型:
【題目】復分解反應存在這樣一個規律:較強酸可制取較弱酸。中和反應、鹽類的水解也是復分解反應,鹽類的水解反應的逆反應是中和反應。鹽類的水解反應中,弱酸強堿鹽中弱酸根離子對應的弱酸越弱,其鹽越容易發生水解。
已知在常溫下測得濃度均為0.lmol/L的下列6種溶液的pH:
溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 8.1 | 11.6 | 10.3 | 11.1 | 11.3 |
(1)請根據上述信息判斷下列反應不能發生的是_____(填編號)。
A ![]()
B ![]()
C ![]()
D ![]()
E ![]()
F ![]()
(2)一些復分解反應的發生還遵循其他的規律、下列變化都屬于復分解反應:
①將石灰乳與純堿溶液混合可制得苛性鈉溶液
②向飽和碳酸氫銨溶液中加入飽和食鹽水可獲得小蘇打固體
③蒸發KC1和NaNO3的混合溶液,首先析出NaCl晶體。
根據上述反應,總結出復分解反應發生的另一規律為_____。
(3)已知溶液的pH與氫離子濃度有直接關系。物質的量濃度均為0.05mol/L的下列五種物質的溶液中,pH由大到小的順序是_____(填編號)。
①C6H5OH(苯酚) ②CH3COOH ③HClO4 ④HC1O ⑤H2SO4
(4)25℃時,M酸溶液的pH=a,N堿溶液的pH=b。若X為強酸,Y為強堿,且![]() ,若兩者等體積混合后,溶液的pH=7.此時溶液中金屬陽離子濃度大于酸根陰離子濃度,其原因可能是_____。
,若兩者等體積混合后,溶液的pH=7.此時溶液中金屬陽離子濃度大于酸根陰離子濃度,其原因可能是_____。
查看答案和解析>>
科目: 來源: 題型:
【題目】已知,標準狀況下二氧化碳的密度可表示為44/22.4g/L。將CO2通入NaOH溶液中,所得產物隨通入的CO2的質量的不同而不同。完成下列填空。
(1)向NaOH溶液中通入CO2,先發生反應_____(用方程式表示),繼續通入,又發生反應_____。
(2)250g質量分數4%的NaOH溶液,最多可吸收CO2的體積為_____L(標準狀況下)。
(3)向250質量分數8%的的NaOH溶液中通入一定量CO2,溶液增重4.4g,將所得溶液蒸干,計算所得固體中各成分以及其質量為_____。
(4)向未知濃度、體積為VL的NaOH溶液中緩緩通入一定體積(標準狀況下)的CO2,充分反應后,CO2和NaOH均無剩余,再向溶液中加入過量的澄清石灰水生成m1g白色沉淀。根據以上數據,用代數式表示CO2的體積V(CO2)=_____。
查看答案和解析>>
科目: 來源: 題型:
【題目】草酸固體熔點較低,受熱熔化后,迅速分解生成三種氧化物。
(1)草酸(H2C2O4)中,氫、碳、氧元素的質量比為_____。
(2)寫出草酸受熱分解的化學方程式:_____。
(3)加熱分解草酸固體,應選擇圖中的_____裝置。
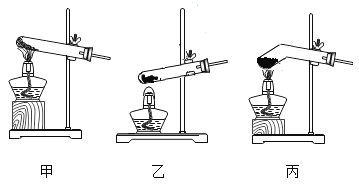
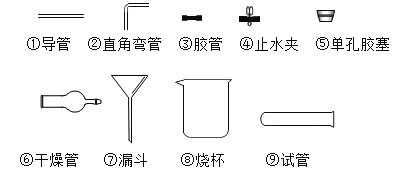
(4)下列儀器可裝配一套“隨開隨用、隨關隨停”的氣體發生裝置。請填寫所用儀器的序號:_____(夾持、固定的儀器不考慮)。能用該套裝置制取的氣體有_____(任填兩種)。
查看答案和解析>>
科目: 來源: 題型:
【題目】如表列出了①~⑥六種元素在周期表中的位置:
族 周期 | IA | |||||||
1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ||||
請按要求回答下列問題:
(1)元素①的元素符號是_____。
(2)元素⑤的原子結構示意圖是_____。
(3)這六種元素中,位于第三周期且原子半徑最小的是(填元素符號)_____。
(4)這六種元素中的金屬元素組成的等質量的碳酸鹽中,與足量稀鹽酸反應放出CO2最多的碳酸鹽的化學式為_____。
(5)在盛有硫酸銅溶液的小燒杯中加入元素③的單質,發生反應的現象是_____。
查看答案和解析>>
科目: 來源: 題型:
【題目】氧化銅與稀鹽酸發生反應時,容器中溶液總質量隨時間的變化曲線如圖所示。下列說法正確的是( )
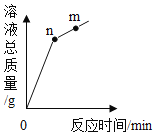
A.該實驗是將氧化銅逐漸加入稀鹽酸中
B.n點和m點對應溶液中銅元素質量分數相等
C.n點和m點對應溶液蒸發結晶后得到的固體成分相同
D.該曲線不能反映溶液中溶劑質量隨時間的變化關系
查看答案和解析>>
科目: 來源: 題型:
【題目】某些鹽在溶液中結晶時,析出的晶體是結晶水合物。下表記錄了t°C時向4份相同的硫酸銅溶液中加入的無水硫酸銅的質量以及析出硫酸銅晶體(CuSO4·5H2O)的質量的實驗數據:
硫酸銅溶液 | Ⅰ | Ⅱ | III | IV |
加入的無水硫酸銅(g) | 2.5 | 4.0 | 6.0 | 8.0 |
析出的硫酸銅晶體(g) | 0.10 | 2.8 | 6.4 | 10.0 |
當加入4.6g無水硫酸銅時,析出硫酸銅晶體的質量為( )
A.2.56gB.3.42g
C.3.88gD.6.82g
查看答案和解析>>
科目: 來源: 題型:
【題目】氧化鈣和過氧化鈣(CaO2)的混合物12.8g溶于足量水后,加入足量的Na2CO3溶液,溶液中的Ca2+全部轉化為沉淀,過濾、干燥,得到20g CaCO3。則原12.8g混合物中鈣元素與氧元素的質量之比為(已知2CaO2+2H2O===2Ca(OH)2+O2↑)( )
A. 5:2 B. 5:3 C. 5:4 D. 1:1
查看答案和解析>>
科目: 來源: 題型:
【題目】已知,同溫、同壓下,相同體積的任何氣體都含有相同數目的分子。如圖所示,相同狀況下,分別用氯化氫和四種不同的混合氣體吹出體積相等的五個氣球。A、B、C、D四個氣球中所含原子數與氯化氫氣球中所含原子數一定相等的是( )
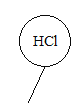
A. 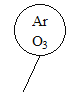 B.
B. 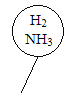 C.
C. 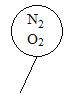 D.
D. 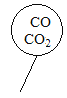
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com