
【題目】利用廢棄白銅(Cu、Ni)分離得到Cu、Ni兩種金屬,其主要流程如下:
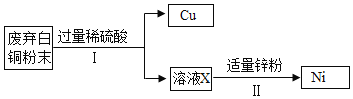
已知:Ni與Fe化學性質相似,常見化合價為+2價。
(1)步驟Ⅰ中反應的化學方程式為_________。
(2)步驟Ⅱ中反應屬于基本反應類型中的_______。
 輕松課堂單元測試AB卷系列答案
輕松課堂單元測試AB卷系列答案 小題狂做系列答案
小題狂做系列答案科目:初中化學 來源: 題型:
【題目】在研究酸和堿的化學性質時,某同學發現稀H2SO4與NaOH溶液混合后無明顯現象產生,于是設計并完成了如下實驗方案。
方案一:測定稀H2SO4與NaOH溶液混合前后的pH.
(1)用pH試紙測定NaOH溶液的pH,測得pH___________7 (選填“大于”、“等于”或“小于”);
(2)將定量的稀H2SO4加入該NaOH溶液中,混合均勻后測定其pH, pH=7。
方案二:向盛有NaOH溶液的燒杯中先滴加酚酞試液,后滴加稀硫酸,觀察到溶液由紅色變成無色。
結論:稀H2SO4與NaOH溶液發生了化學反應;
在上述實驗中需要用到溶質質量分數為10%的稀硫酸,現用20g溶質質量分數為98%的濃硫酸進行稀釋,則需要增加水的質量為________g, 若實驗過程中量水時仰視讀數,則會造成所得溶液溶質質量分數_____(選填“偏大”、“不變”或“偏小”)
(3)甲酸(HCOOH)是一種具有揮發性的酸, 甲酸在熱的濃硫酸中會分解生成兩種氧化物;CO和H2O。如圖是制取CO,用CO還原氧化鐵并檢驗氣體產物,同時收集尾氣中的CO的實驗裝置。
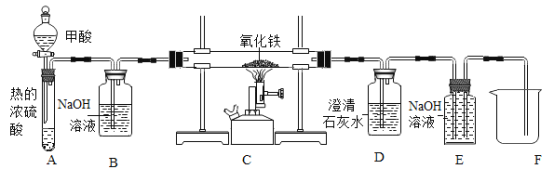
①寫出E裝置玻璃管內發生反應的化學方程式______。
②若沒有B裝置,則不能達到檢驗氣體產物的目的,原因是_____。
③E裝置可起到收集CO的作用,實驗結束時,E中有部分溶液進入到F燒杯中,請設計實驗證明該溶液溶質的成分中含有NaOH,寫出實驗步驟、現象和結論__。
(4)某特種鋼村需要用富鐵礦石(含鐵量高于50%)來冶煉。研學實踐小組為測出某地赤鐵礦石(主要成分是Fe2O3)中的含鐵量,進行實驗:取20g赤鐵礦石樣品,逐漸加入稀鹽酸,充分反應。實驗相關數據如圖所示(假設雜質不溶于水,也不與酸反應)。請計算:
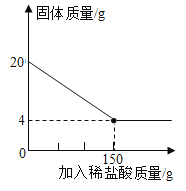
①20g赤鐵礦石樣品中氧化鐵的質量_____。
②計算該樣品中鐵元素的質量分數,由此判斷該赤鐵礦石是否屬于富鐵礦石_____。
③實驗中所用稀鹽酸溶質的質量分數_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室制取、收集、干燥氣體的常用裝置如下圖所示。請回答下列問題:
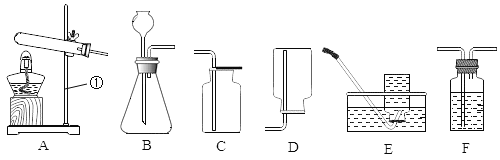
(1)寫出圖中標有序號的儀器名稱:①_____;
(2)實驗室用高錳酸鉀制取氧氣的發生裝置應該選用___(填字母序號),該反應的化學方程式為______________;
(3)氧氣可用排水法收集,是因為_________,某同學用排水法收集了一瓶氧氣,在做“鐵絲在氧氣中燃燒”時,鐵絲沒有燃燒,你認為可能的原因是__________;
(4)實驗室制取二氧化碳氣體的收集裝置應選用___(填字母序號),要除去二氧化碳中混有的水蒸氣,F裝置中的試劑是______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】化學與生活息息相關。
(1)含硫的煤燃燒時會產生污染空氣的_____________ (填物質名稱或化學式,下同) ;用煤爐取暖時易發生中毒,主要是由于室內_____________排放不暢引起的。
(2)凈水器中經常使用活性炭,主要是利用活性炭的_____________性。
(3)“ 合理膳食,均衡營養”會讓我們更健康。
①某同學午餐食譜中有:米飯、饅頭、紅燒牛肉、清蒸魚,根據你所學的知識,
從合理膳食的角度建議應該增加的食物是___________(填字母序號)。
a.  蒸雞蛋
蒸雞蛋
b.  方便面
方便面
c.  涼拌黃瓜
涼拌黃瓜
d.  粉蒸肉
粉蒸肉
②為了預防佝僂病,幼兒及青少年可以補充一些含______________元素的食品。
(4)下列日常生活中的做法,符合“低碳生活”理念的是_____________。
a.節約使用紙張
b.分類回收處理垃圾
c.減少使用塑料袋
d.減少使用一次性紙杯
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲、乙兩種固體的溶解度曲線如下圖所示。下列說法中,不正確的是
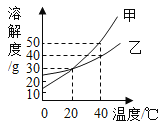
A.20℃時,甲、乙兩種物質的溶解度相等
B.40℃時,甲的飽和溶液中溶質和溶劑的質量比為1:2
C.升高溫度可以將甲、乙的飽和溶液轉化為不飽和溶液
D.40℃時,向100g水中加入50g乙,所得溶液溶質質量分數為33.3%
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】利用如下圖所示步驟進行實驗,其中不能達到實驗目的的是( )
實驗目的 | 實驗步驟 | |
A | 比較鐵、銅的金屬活動性強弱 | ①加入銅粉末;②加入適量稀硫酸攪拌;③加入鐵片 |
B | 檢驗NaCl中混有Na2CO3 | ①加入少量樣品;②加入適量水至全部溶解; ③加入適量稀鹽酸 |
C | 驗證KCl不能無限溶解 | 20°C時,①加入100g水;②加入18gKCl攪拌;③加入16gKCl攪拌(已知:20℃時,KCl的溶解度為34g) |
D | 配置50g溶質質量分數為5%的氯化鈉溶液 | ①加入2.5gNaCl;②加入47.5g水;③攪拌至全部溶解 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】現代工業常以氯化鈉、二氧化碳、氨氣(NH3)為原料制備碳酸鈉,主要流程如下:
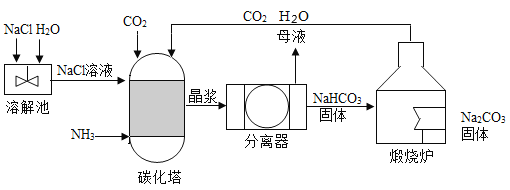
注:晶漿中主要含有NaHCO3固體、NaCl溶液、NH4Cl溶液;母液是含有NaCl、NH4Cl的溶液。
(1)溶解池中,NaCl溶于水的過程中需不斷攪拌,其目的是_____。
(2)煅燒爐中發生反應的基本反應類型為_____。
(3)整個流程中,可以循環使用的物質有_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖是探究鐵銹蝕條件的裝置,實驗開始時L端與R端的液面高度一致。
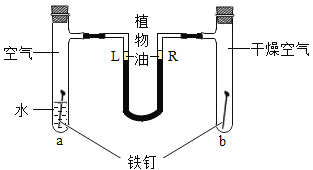
(1)一周后可觀察到_______(填“L”或“R”)端液面上升。
(2)有人提議將鐵釘換作與鐵釘質量相等的細鐵粉來縮短實驗天數,理由是_____。
(3)該實驗______(寫“能”或“不能”)證明鐵生銹與氧氣有關。理由是_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲、乙兩種物質(均不含結晶水)的溶解度曲線如圖所示,請回答。
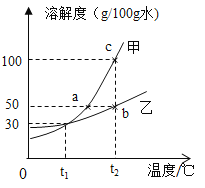
①t2°C時,甲物質的溶解度是_____。
②t1°C時,100g水中放入50g乙,充分溶解后所得溶液的質量是_____g。
③t2°C時,取100g甲、乙固體分別配成飽和溶液,所需水較少的是_____(填“甲”或“乙”);分別降溫到t1°C,甲析出晶體質量比乙多_____g。
④甲溶液狀態發生改變時,操作正確的是_____。
A a點→c點:加熱
B b點→c點:恒溫蒸發
C a點→b點:加水
D c點→a點:降溫、過濾
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com