
【題目】在學習了稀鹽酸和稀硫酸的化學知識后,同學們發現實驗室中還有兩瓶濃硫 酸和濃硝酸,為了進一步了解酸的有關知識,將同學分為甲、乙兩組進行探究
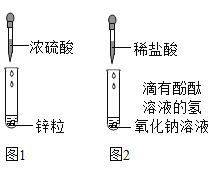
(1)甲組的同學做了如圖1所示實驗,發現有刺激性氣味的氣體生成,請你完成化學反應方程式:Zn+2H2SO4(濃)=ZnSO4+___↑+2H2O.反應一段時間后,老師提醒還可能生成另一種氣體.大家都很好奇,這是什么氣體呢?請你根據酸的化學性質,推斷此氣體可能是___,其理由是___.
(2)乙組的同學打開盛裝濃硝酸的試劑瓶,觀察到瓶口有白霧產生.據此可知,濃硝酸具有_______(填一條物理性質).乙組同學又取少量濃硝酸置于試管中,采用強光照射或者稍加熱,立即觀察到溶液上方有紅棕色的NO2氣體產生.據此現象可推知濃硝酸具有______(填一條化學性質).實驗室應如何保存濃硝酸?_______.
【答案】SO2 氫氣或H2 隨著硫酸的消耗和水的生成,濃硫酸變成稀硫酸,鋅和稀硫酸反應生產氫氣 揮發性 受熱易分解 棕色瓶陰冷處保存
【解析】
(1)根據質量守恒定律可知,濃硫酸和鋅反應生成硫酸鋅、二氧化硫和水,化學反應方程式:Zn+2H2SO4(濃)=ZnSO4+SO2↑+2H2O;隨著硫酸的消耗和水的生成,濃硫酸變成稀硫酸,鋅和稀硫酸反應生產氫氣,所以還可能生成另一種氣體就是氫氣;故填:SO2;氫氣或H2;隨著硫酸的消耗和水的生成,濃硫酸變成稀硫酸,鋅和稀硫酸反應生產氫氣。
(2)打開盛裝濃硝酸的試劑瓶,觀察到瓶口有白霧產生.據此可知,濃硝酸具有揮發性,又取少量濃硝酸置于試管中,采用強光照射或者稍加熱,立即觀察到溶液上方有紅棕色的NO2氣體產生.據此現象可推知濃硝酸具有受熱易分解,實驗室保存濃硝酸要放在棕色瓶陰冷處保存.故填:揮發性;受熱易分解;棕色瓶陰冷處保存。


科目:初中化學 來源: 題型:
【題目】鐵鍋、鋁鍋是生活中常用的炊具,下圖是鐵鍋的示意圖。
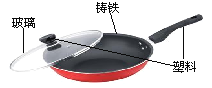
(1)鐵鍋含有的金屬單質___________(寫化學式)。
(2)炒菜時鐵鍋中的油著火可用鍋蓋蓋滅,其原理是________________________。
(3)鋁鍋輕便、耐用,其原因是________________________。
(4)廢舊鐵鍋、鋁鍋不要隨意丟棄,應回收利用,這樣做的意義是____________________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】構成物質的粒子之間的關系如右圖所示。
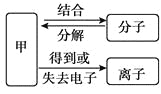
(1)甲是_____。
(2)氧氣、汞和氯化鈉3種物質中,由離子構成的是______。
(3)某粒子的結構示意圖為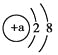 。
。
① 當a=___時,該粒子是原子;② 當a=11時,該粒子的符號為____。
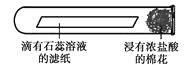
(4)如右圖所示,將滴有石蕊溶液的濾紙放入試管中,試管口放置一浸有濃鹽酸的棉花,可觀察到的現象是______, 此現象說明分子具有的性質是_______。
(5)下圖為某反應的部分微觀示意圖,其中不同的球代表不同元素的原子。
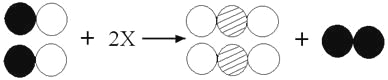
請畫出X分子的微觀示意圖:________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為研究物質的溶解與結晶,在實驗室某同學將100g KNO3放入60℃的100g水中,充分溶解后得溶液甲,然后對該溶液進行如下操作:
![]()
根據下圖KNO3的溶解度曲線,請回答:
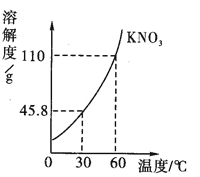
(1)60℃KNO3的溶解度為______________
(2)溶液乙的質量為__________g,丙、丁溶液溶質的質量分數關系是丙___丁(填“<”、>”、“=”)以上四種溶液屬于不飽和溶液的是________。
(3)通過以上實驗可知,結晶的方法通常有_____________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(1)西漢劉安所著《淮南萬畢術》中有“曾青得鐵則化為銅”(銅指銅單質)的記載,這里的曾青是硫酸銅,那么這里的鐵為______________ (填“鐵的單質”或“鐵的化合物”)。
(2)環氧乙烷是美英聯軍對伊拉克的軍事打擊中使用的一種炸彈彈藥的成分之一。環氧乙烷(用字母X代表)完全燃燒的化學方程式為 ,則環氧乙烷的化學式為______________。
,則環氧乙烷的化學式為______________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下圖中,四位同學正在討論某一個化學方程式表示的意義,他們所描述的化學方程式是( )

A. S + O2![]() SO2B. 2CO + O2
SO2B. 2CO + O2![]() 2CO2
2CO2
C. 2H2 + O2![]() 2H2OD. CH4 +2O2
2H2OD. CH4 +2O2![]() CO2 + 2H2O
CO2 + 2H2O
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】配平下列化學方程式:
(1)_____C2H2+_____O2  _____CO2+_____H2O
_____CO2+_____H2O
(2)_____Fe2O3+_____H2  _____Fe+_____H2O
_____Fe+_____H2O
(3)_____Al2O3+_____H2SO4=_____Al2(SO4)3+_____H2O
(4)_____Na+_____H2O=_____NaOH+_____H2↑
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】近期,某公司員工在租住某品牌公寓數月后,查出患白血病,隨后病情惡化去世的事件,引發了各界關注,矛頭直指室內甲醛污染。我國現行的室內空氣監管標準主要有兩種,其中具有強制性的是由建設部、國家質量監督檢驗檢疫總局聯合頒布的![]() 民用建筑工程室內環境污染控制規范
民用建筑工程室內環境污染控制規范![]() ,規定包括住宅、醫院、老年建筑、幼兒園、學校教室等在內的Ⅰ類民用建筑工程,甲醛濃度限量
,規定包括住宅、醫院、老年建筑、幼兒園、學校教室等在內的Ⅰ類民用建筑工程,甲醛濃度限量![]() 。客觀而言,白血病與甲醛污染是否有直接聯系,目前尚未有定論。甲醛化學式為HCHO,本身無色、帶有刺激性氣味,在室溫下極易揮發,但一般只有甲醛超標兩到三倍以上,才能引起人們的感官察覺。不是說室內沒有味道就不存在甲醛污染,單憑嗅覺來判斷是不充分的。另一方面,新家的味道還包括TVOC或者苯系物的味道。所以有味道就是有甲醛污染,是錯誤的認知。清華大學環境學院曾就民間流傳去除甲醛的“土方法”做過實驗:分別將一定量的剩茶葉、新鮮柚子皮、綠蘿、活性炭放入甲醛超標模擬實驗室。測試發現利用這些生活小物去除甲醛的確有效果,但效果微乎其微。科學家認為,避免室內甲醛超標最經濟有效的方法就是開窗通風。至于加速甲醛釋放的方法,因為甲醛釋放與室內溫度和濕度相關,可利用空調提高室內溫度和濕度加速甲醛釋放。甲醛在有氧化性物質存在的條件下,能被氧化為甲酸
。客觀而言,白血病與甲醛污染是否有直接聯系,目前尚未有定論。甲醛化學式為HCHO,本身無色、帶有刺激性氣味,在室溫下極易揮發,但一般只有甲醛超標兩到三倍以上,才能引起人們的感官察覺。不是說室內沒有味道就不存在甲醛污染,單憑嗅覺來判斷是不充分的。另一方面,新家的味道還包括TVOC或者苯系物的味道。所以有味道就是有甲醛污染,是錯誤的認知。清華大學環境學院曾就民間流傳去除甲醛的“土方法”做過實驗:分別將一定量的剩茶葉、新鮮柚子皮、綠蘿、活性炭放入甲醛超標模擬實驗室。測試發現利用這些生活小物去除甲醛的確有效果,但效果微乎其微。科學家認為,避免室內甲醛超標最經濟有效的方法就是開窗通風。至于加速甲醛釋放的方法,因為甲醛釋放與室內溫度和濕度相關,可利用空調提高室內溫度和濕度加速甲醛釋放。甲醛在有氧化性物質存在的條件下,能被氧化為甲酸![]() 。甲酸進一步的分解產物為二氧化碳和水。
。甲酸進一步的分解產物為二氧化碳和水。
綜合上述材料,回答下列問題:
(1)規定包括住宅、醫院、老年建筑、幼兒園、學校教室等在內的Ⅰ類民用建筑工程,甲醛濃度限__。
(2)甲醛是由_______元素組成,它們的原子個數比是_______。
(3)新房裝修,避免室內甲醛超標最經濟有效的方法是____,而加速甲醛釋放,可采取的措施是___。
(4)請寫出甲酸分解的符號表達式_______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(1)在春秋戰國時期,我國就開始生產和使用鐵器,鋼的質量也達到較高水平。古代,人們把燒紅的生鐵放在鐵砧上反復錘打,最終使生鐵轉化為鋼,用化學方程式表示原理 。
(2)工業上用一氧化碳和赤鐵礦煉鐵的化學方程式是_______________________。
(3)新型材料納米鐵粉具有廣泛的用途,它比普通鐵粉更易與氧氣反應,其制備的主要流程如下圖所示。
![]()
納米級鐵粉遇氧氣無需加熱就能燃燒,生成物的化學式為 。
高溫反應器中發生反應的化學方程式為 。反應前需向反應器中通入氮氣,目的是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com