
【題目】鋁是重要的輕金屬,廣泛應用于航空、電訊和建筑等領域。
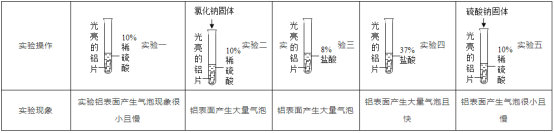
(1)依據金屬的活動性順序,鋁的金屬活動性比鋅__________.但是將鋁片和鋅粒分別投入稀硫酸中,鋁片表面產生的氣泡卻比鋅粒少而慢。為了探究影響鋁與酸反應速率的因素,振興同學用相同質量、相同形狀、除去氧化膜的鋁片設計如圖所示實驗。
(2)寫出實驗中發生反應的化學方程式_______________________________________.
(3)比較實驗三、四說明鋁與酸反應產生氫氣的速率,與_____________________有關.
(4)比較實驗一、二說明鋁與酸反應產生氫氣的速率,可能與_________、_________(填粒子符號)、與和溫度、金屬與酸的接觸面積等各種因素有關。
(5)比較實驗一、二、五可以得出的結論是____________________________________.
【答案】強 2Al+3H2SO4=Al2(SO4)3+3H2↑ 鹽酸濃度(或鹽酸溶質質量分數) Na+ Cl- Cl-能加快酸與活潑金屬的反應速率
【解析】
(1)在金屬活動性順序中,鋁位于鋅的前面,故活動性鋁比鋅強,即鋁比鋅活潑。
(2)鋁和硫酸反應生成硫酸鋁和氫氣;化學方程式為:2Al+3H2SO4=Al2(SO4)3+3H2↑;
(3)比較實驗三、四,除酸的濃度不同,其他因素都相同,可得出鋁與酸反應產生氫氣的速率與酸的濃度有關;
(4)比較實驗一、二,不同之處是實驗二中加入了NaCl固體,從而導致產生氣泡的速率加快,因此鋁與酸反應產生氫氣的速率,可能與構成氯化鈉的粒子--鈉離子、氯離子有關;
(5)由實驗一、二、五的實驗現象可知,氯化鈉中的氯離子可以加快金屬與酸的反應速率,而硫酸鈉中的硫酸根離子不能加快金屬與酸的反應速率。


科目:初中化學 來源: 題型:
【題目】(9分)某化學小組利用如圖所示裝置(圖中固定裝置已略去)測定銅鋅合金中鋅的質量分數.
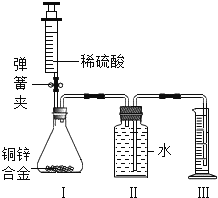
探究過程如下:
①連接實驗裝置并檢查裝置氣密性.
②向裝置Ⅰ中的錐形瓶加入2.0g的銅鋅合金樣品粉末,由注射器緩緩注入稀硫酸,待到錐形瓶中不再產生氣體時,準確讀取注射器內讀數,減少10.5mL稀硫酸,同時立即夾緊彈簧夾,移出裝置Ⅲ中的導管,準確讀取量筒內水的體積為214.0mL.(注:樣品中的雜質不參加反應)
③裝置Ⅰ中剩余固體物質經過適當處理后,準確稱量其質量1.4g.
④該小組的三位同學利用實驗過程測得不同數據,計算銅鋅合金樣品中鋅的質量分數.
甲同學利用裝置Ⅰ中反應前后固體的質量進行計算;
乙同學利用裝置Ⅰ中加入稀硫酸的量進行計算;
丙同學利用裝置Ⅲ中量取水的體積進行計算,并查得:在標準狀況下,氫氣的密度為0.09g/L.
回答下列問題:
(1)裝置Ⅰ中反應的化學方程式為 ,實驗過程中須加入稀硫酸至不再產生氣體,目的是 .
(2)步驟③中稱量剩余固體之前的正確操作是 、洗滌、干燥.
(3)根據實驗測定的數據,上述三位同學中 (填“甲”、“乙”或“丙”)同學無法進行計算樣品中鋅的質量分數.
(4)化學小組同學發現:按照丙同學的方案進行計算,致使實驗結果出現較大偏差.以下因素可能造成偏差的有 (填標號).
A.移出裝置Ⅲ時,導管內留存了一部分水
B.實驗測量前,沒有排除裝置Ⅰ中的空氣
C.數據處理時,未排除加入稀硫酸所占的體積.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】從“生活走進化學,從化學走向社會”是化學學習的重要理念。
(1)下列物質放入水中溫度明顯下降的一種是________(填寫序號):
A.食鹽 B.硝酸銨 C.氫氧化鈉 D.蔗糖
(2)使用乙醇汽油可有效緩解汽車尾氣污染,請寫出乙醇燃燒的化學方程式____________。
(3)“節能減排,建設創新型國家”是我國基本國策。下列行為能體現這一理念的是________(填序號)。
A.大力開發新能源,減少溫室氣體排放;
B.進行技術創新,淘汰產能落后、污染重的化工企業;
C.合理使用化肥農藥,走可持續發展的農業生產之路;
D.發展低碳經濟,倡導綠色出行。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據下列實驗裝置圖,回答下列問題。
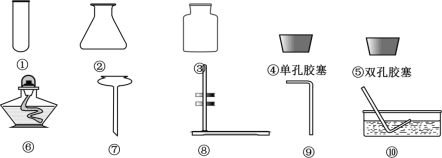
(1)寫出圖中儀器的名稱:③____________。
(2)小明用高錳酸鉀制取并收集干燥的氧氣,他應從上圖儀器中選擇____(填序號)組裝一套裝置。但圖中還少一樣儀器,這種儀器名稱是_______。
(3)寫出用高錳酸鉀制取氧氣的化學反應方程式_________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖所示進行有關碳及其氧化物的性質實驗,錯誤的說法是:
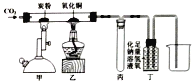
A. 玻璃管內的炭粉減少、氧化銅由黑變紅
B. 甲處發生的反應是一個典型的吸熱反應
C. 該裝置的不足之處是沒有進行尾氣處理
D. 丙處的試管可以防止液體倒吸入玻璃管
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】A—J都是初中化學常用的物質。其中B、E、H、J是單質,其余均為化合物,氣體C可用于滅火。“C→B”的轉化過程,在自然界中稱為光合作用。它們相互間的轉化關系如下圖所示(部分反應物、生成物及反應條件已略去)。
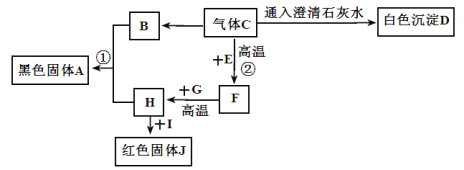
請回答下列問題:
(1)寫出物質D、J的化學式:D___________,J___________。
(2)反應①的反應條件___________,其基本反應類型___________。
(3)寫出反應②的化學方程式:______________________。
(4)若要實現“H+I→紅色固體J”的轉化,物質I可能是___________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為測定某樣品(碳酸鈉和氯化鈉的混合物)中碳酸鈉的質量分數,某化學興趣小組進行以下實驗,取50g的樣品放置于燒杯中,然后取一定溶質質量分數的稀鹽酸100g,加入到裝樣品的燒杯中,恰好完全反應得到132.4g溶液。求:
(1)樣品中碳酸鈉的質量分數是________(精確到0.1%)。
(2)所用稀鹽酸的溶質質量分數________(寫出具體的計算過程)。
(3)所得溶液的溶質質量分數________(寫出具體的計算過程)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】水和溶液在生產、生活中起著十分重要的作用,請回答下列問題。
(1)請完成鑒別硬水和軟水的實驗報告。
實驗步驟 | 實驗現象及結論 |
___ | ___ |
(2)電解水實驗裝置如圖甲所示,a管產生的氣體是___,用燃著的木條靠近該管尖嘴處,打開活塞,可觀察到的現象___。
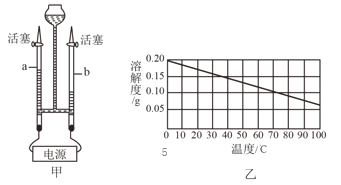
(3)圖乙是氫氧化鈣的溶解度曲線。40℃時,氫氧化鈣的溶解度是0.14g,這句話的含義是___。將室溫下的飽和氫氧化鈣溶液升溫(不超過100℃),發現氫氧化鈣溶液變渾濁,請根據溶解度曲線解釋原理:___。
(4)某石灰水含有氫氧化鈣1.48g,要使該石灰水中的氫氧化鈣全部轉化為碳酸鈣沉淀,至少需要二氧化碳的質量是_____?(請在答題紙上寫出完整的解題過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某氫氧化鈉樣品中混有氯化鈉,為測定樣品中氫氧化鈉的質量分數,稱取5 g樣品,加入27 g水完全溶解后,緩慢加入稀鹽酸,同時測定溶液的pH。當pH=7時,剛好用去10%的稀鹽酸36.5 g。試計算:
(1)將100 g質量分數為38%的濃鹽酸稀釋成10%的稀鹽酸,需加水的質量為 g。
(2)樣品中氫氧化鈉的質量分數。
(3)反應后所得溶液中溶質的質量分數。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com